题目内容
某化学兴趣小组提出可以用含铜废料制备蓝色胆矾(CuSO4?XH2O).查阅资料:
Ⅰ.过氧化氢常温下会缓慢分解为氧气和水.对其水溶液加热、光照或加催化剂(如MnO2)都促进其分解.
Ⅱ.CuSO4?XH2O易溶于水难溶于酒精,加热时会逐步失去结晶水,最终生成CuSO4.
Ⅲ.白色粉末CuSO4易与水化合生成CuSO4?XH2O
I.酸铜晶体的制备
方案1:毛毛同学根据已学知识,提出了制备硫酸铜方案:
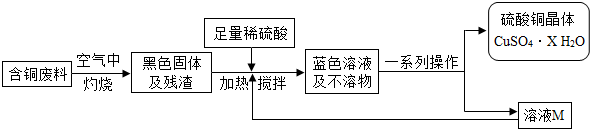
方案2:方舟同学查阅资料归纳了一种工业制备硫酸铜的流程:
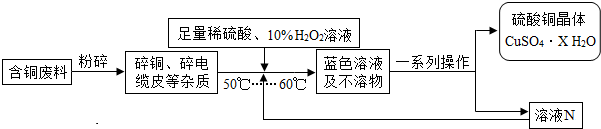
(1)上述方案1中加热搅拌的作用是 ,形成蓝色溶液的化学反应方程式是: .
(2)方案2中,加入H2O2后要求温度控制在50℃到60℃是为了防止 .
(3)从环保角度对两套方案的不同部分进行比较,你认为方案 (填1或2)更合理.理由是 .
(4)方案中“一系列操作”依次为:过滤、 、冷却结晶、 (填序号).
A.蒸发浓缩 B.加水稀释 C.加水溶解 D.过滤
(5)溶液M、N都是CuSO4的 (选填a“饱和”、b“不饱和”或c“不一定饱和”)溶液.
(6)所得硫酸铜晶体需要洗涤后晾干,最合适的洗涤试剂是 .
A.冷蒸馏水 B.95%的酒精 C.热蒸馏水
Ⅱ.酸铜晶体(CuSO4?xH2O)中结晶水(xH2O)含量测定学习小组取12.5g硫酸铜晶体(CuSO4?xH2O)进行加热分解,获得相关数据,并绘制成固体质量与温度的关系图.
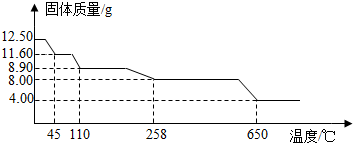
(7)258℃时,固体完全变成白色粉末.根据图中数据,计算CuSO4?xH2O中x的值为 .
加热过程中,硫酸铜晶体分步失去结晶水.请写出45℃到110℃时反应方程式: .
(8)580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为 .
Ⅰ.过氧化氢常温下会缓慢分解为氧气和水.对其水溶液加热、光照或加催化剂(如MnO2)都促进其分解.
Ⅱ.CuSO4?XH2O易溶于水难溶于酒精,加热时会逐步失去结晶水,最终生成CuSO4.
Ⅲ.白色粉末CuSO4易与水化合生成CuSO4?XH2O
I.酸铜晶体的制备
方案1:毛毛同学根据已学知识,提出了制备硫酸铜方案:

方案2:方舟同学查阅资料归纳了一种工业制备硫酸铜的流程:

(1)上述方案1中加热搅拌的作用是
(2)方案2中,加入H2O2后要求温度控制在50℃到60℃是为了防止
(3)从环保角度对两套方案的不同部分进行比较,你认为方案
(4)方案中“一系列操作”依次为:过滤、
A.蒸发浓缩 B.加水稀释 C.加水溶解 D.过滤
(5)溶液M、N都是CuSO4的
(6)所得硫酸铜晶体需要洗涤后晾干,最合适的洗涤试剂是
A.冷蒸馏水 B.95%的酒精 C.热蒸馏水
Ⅱ.酸铜晶体(CuSO4?xH2O)中结晶水(xH2O)含量测定学习小组取12.5g硫酸铜晶体(CuSO4?xH2O)进行加热分解,获得相关数据,并绘制成固体质量与温度的关系图.

(7)258℃时,固体完全变成白色粉末.根据图中数据,计算CuSO4?xH2O中x的值为
加热过程中,硫酸铜晶体分步失去结晶水.请写出45℃到110℃时反应方程式:
(8)580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为
考点:物质的相互转化和制备,饱和溶液和不饱和溶液,金属的化学性质,酸的化学性质,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:物质的制备
分析:(1)根据方案1中加热搅拌的作用是加快反应速率,同时使反应进行更彻底以及氧化铜和硫酸反应生成硫酸铜和水进行解答;
(2)根据方案2中,加入H2O2后要求温度控制在50℃到60℃是为了防止H2O2受热分解进行解答;
(3)根据两个方案的比较,看是否有污染或考虑产量问题;
(4)根据得到硫酸铜晶体需要的步骤进行解答;
(5)根据有晶体析出,说明该溶液是饱和溶液进行解答;
(6)根据用水洗涤可以溶解硫酸铜晶体,使硫酸铜晶体有损失进行解答;
(7)根据由图示数据和“到t1℃时该固体完全失去结晶水”可知,结晶水的质量为:12.50g-8.0g=4.5g,根据结晶水的质量计算出硫酸铜晶体中结晶水的个数;根据加热过程中,硫酸铜晶体分步失去结晶水.所以45℃到110℃时是三水硫酸铜受热分解生成一水硫酸铜和水进行解答;
(8)根据580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物氧化铜、二氧化硫及氧气进行解答.
(2)根据方案2中,加入H2O2后要求温度控制在50℃到60℃是为了防止H2O2受热分解进行解答;
(3)根据两个方案的比较,看是否有污染或考虑产量问题;
(4)根据得到硫酸铜晶体需要的步骤进行解答;
(5)根据有晶体析出,说明该溶液是饱和溶液进行解答;
(6)根据用水洗涤可以溶解硫酸铜晶体,使硫酸铜晶体有损失进行解答;
(7)根据由图示数据和“到t1℃时该固体完全失去结晶水”可知,结晶水的质量为:12.50g-8.0g=4.5g,根据结晶水的质量计算出硫酸铜晶体中结晶水的个数;根据加热过程中,硫酸铜晶体分步失去结晶水.所以45℃到110℃时是三水硫酸铜受热分解生成一水硫酸铜和水进行解答;
(8)根据580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物氧化铜、二氧化硫及氧气进行解答.
解答:解:(1)方案1中加热搅拌的作用是加快反应速率,同时使反应进行更彻底;铜灼烧后变成氧化铜,氧化铜与硫酸反应生成硫酸铜和水,所以方程式是:CuO+H2SO4═CuSO4+H2O;
(2)H2O2受热易分解,温度应该控制在50℃到60℃之间,防止H2O2受热分解;
(3)从环保角度对两套方案的不同部分进行比较,甲方案第一步灼烧会产生污染空气的气体,粉尘,烟雾,由此可知方案2更合理;
(4)方案中“一系列操作”依次为:过滤、蒸发浓缩、冷却结晶、过滤得到硫酸铜晶体;
(5)有晶体析出,说明该溶液是饱和溶液,所以溶液M、N都是CuSO4的饱和溶液;
(6)用水洗涤可以溶解硫酸铜晶体,使硫酸铜晶体有损失,所以所得硫酸铜晶体需要洗涤后晾干,最合适的洗涤试剂是95%的酒精;
(7)由图示数据和“到t1℃时该固体完全失去结晶水”可知,结晶水的质量为:12.50g-8.0g=4.5g
CuSO4?xH2O
CuSO4+xH2O↑.
160+18x 18x
12.50g 4.5g
=
160+18x=50x
x=5;
(8)加热过程中,硫酸铜晶体分步失去结晶水.所以45℃到110℃时是三水硫酸铜受热分解生成一水硫酸铜和水,反应方程式为:CuSO4?3H2O
CuSO4?H2O+2H2O↑;
(9)580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物氧化铜、二氧化硫及氧气,反应方程式为:2CuSO4
2CuO+2SO2↑+O2↑.
故答案为:(1)加快反应速率,同时使反应进行更彻底; CuO+H2SO4═CuSO4+H2O;
(2)H2O2受热分解;
(3)2;避免灼烧废料产生的污染;
(4)A;D;
(5)饱和;
(6)B;
(7)5;
(8)CuSO4?3H2O
CuSO4?H2O+2H2O↑;
(9)2CuSO4
2CuO+2SO2↑+O2↑.
(2)H2O2受热易分解,温度应该控制在50℃到60℃之间,防止H2O2受热分解;
(3)从环保角度对两套方案的不同部分进行比较,甲方案第一步灼烧会产生污染空气的气体,粉尘,烟雾,由此可知方案2更合理;
(4)方案中“一系列操作”依次为:过滤、蒸发浓缩、冷却结晶、过滤得到硫酸铜晶体;
(5)有晶体析出,说明该溶液是饱和溶液,所以溶液M、N都是CuSO4的饱和溶液;
(6)用水洗涤可以溶解硫酸铜晶体,使硫酸铜晶体有损失,所以所得硫酸铜晶体需要洗涤后晾干,最合适的洗涤试剂是95%的酒精;
(7)由图示数据和“到t1℃时该固体完全失去结晶水”可知,结晶水的质量为:12.50g-8.0g=4.5g
CuSO4?xH2O
| ||
160+18x 18x
12.50g 4.5g
| 160+18x |
| 12.50g |
| 18g |
| 4.5g |
160+18x=50x
x=5;
(8)加热过程中,硫酸铜晶体分步失去结晶水.所以45℃到110℃时是三水硫酸铜受热分解生成一水硫酸铜和水,反应方程式为:CuSO4?3H2O
| ||
(9)580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物氧化铜、二氧化硫及氧气,反应方程式为:2CuSO4
| ||
故答案为:(1)加快反应速率,同时使反应进行更彻底; CuO+H2SO4═CuSO4+H2O;
(2)H2O2受热分解;
(3)2;避免灼烧废料产生的污染;
(4)A;D;
(5)饱和;
(6)B;
(7)5;
(8)CuSO4?3H2O
| ||
(9)2CuSO4
| ||
点评:该题为硫酸铜的知识为线索,考查了多方面的知识,综合性很强,难度较大.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
下列情况中,所采取的灭火方法不恰当的是( )
| A、用嘴吹灭蜡烛 |
| B、红磷着火用沙土扑灭 |
| C、电器因短路起火时,用水浇灭 |
| D、炒菜时油锅着火,立即盖上锅盖 |
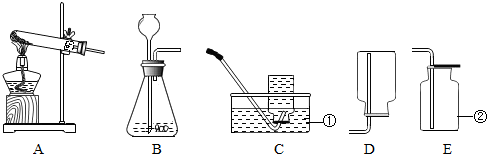

 如示某些物质间转化关系.其中A、E、G为固体,且A、G均为单质,E为红棕色固体,G为常见金属;C、F、D、H为无色气体,其中C、F是由相同元素组成的无色气体,且C有毒;B为常见的无色液体,I为有机物.请回答下列问题:
如示某些物质间转化关系.其中A、E、G为固体,且A、G均为单质,E为红棕色固体,G为常见金属;C、F、D、H为无色气体,其中C、F是由相同元素组成的无色气体,且C有毒;B为常见的无色液体,I为有机物.请回答下列问题: 小刚在化学课上学习了《空气中氧气含量的探究实验》的内容后,非常感兴趣,课后他设计了一套简易装置继续进行探究:将橡皮塞塞紧后的试管体积5等分,做好标记.在试管中加入一小块白磷,用橡皮塞塞紧试管口;等白磷燃烧熄灭后,将试管倒立于盛有水的水槽中(如图),并在水下将橡皮塞取下.请你根据他的探究回答下列问题.
小刚在化学课上学习了《空气中氧气含量的探究实验》的内容后,非常感兴趣,课后他设计了一套简易装置继续进行探究:将橡皮塞塞紧后的试管体积5等分,做好标记.在试管中加入一小块白磷,用橡皮塞塞紧试管口;等白磷燃烧熄灭后,将试管倒立于盛有水的水槽中(如图),并在水下将橡皮塞取下.请你根据他的探究回答下列问题.