题目内容
16.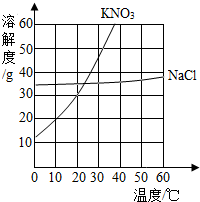 结合图中KNO3和NaCl的溶解度曲线,回答下列问题.
结合图中KNO3和NaCl的溶解度曲线,回答下列问题.(1)温度升高时,溶解度明显增大的是KNO3;
(2)10℃时的将15g的NaCl放入50g水中,充分溶解后,所得溶液为NaCl的不饱和(填“饱和”或“不饱和”)溶液;
(3)要将KNO3从其饱和溶液中的全部结晶出来,应该采用的方法是蒸发溶剂(填“冷却热饱和溶液”或“蒸发溶剂”)
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)根据图示可以看出,温度升高时,溶解度明显增大的是硝酸钾,故填:KNO3;
(2)10℃时,氯化钠的溶解度为35g,将15g的NaCl放入50g水中,充分溶解后,全部溶解,故所得溶液为NaCl的不饱和溶液,故填:不饱和;
(3)要将KNO3从其饱和溶液中的全部结晶出来,应该采用蒸发溶剂的方法,故填:蒸发溶剂.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列化肥中,属于复合肥的是( )
| A. | KCl | B. | NH4Cl | C. | KNO3 | D. | Ca3(PO4)2 |
1.通过下列实验操作和现象能得出相应结论的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向收集满 CO2的软塑料瓶中加入约$\frac{1}{3}$体积滴有石蕊试液的水,旋紧瓶盖,振荡 | 塑料瓶变瘪, 溶液变红 | CO2能与石蕊反应 |
| B | 往CuSO4和FeSO4的混合溶液中加锌粉反应后过滤,在滤渣中滴加稀盐酸 | 有气泡 | 滤渣中一定有Cu和Fe,可能有Zn |
| C | 在某无色溶液中滴加氯化钡溶液 | 有白色沉淀 | 无色溶液中一定含有 Ag+离子 |
| D | 把质量相同的镁条与锌粒同时放入相同浓度和体积的盐酸中 | 镁条与盐酸 产生气体更快 | 镁的金属活动性比锌强 |
| A. | A | B. | B | C. | C | D. | D |
8.逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
| A. | 金刚石和石墨都是碳单质,所以性质都相同 | |
| B. | KNO3属于复合肥,所以K2SO4也属于复合肥 | |
| C. | 某物质中加入稀盐酸,有气泡产生,可证明该物质一定是活泼金属 | |
| D. | 蜡烛燃烧后,虽然质量减少,但是仍然符合质量守恒定律 |
5.下列物质露置于空气中,易发生变质的是( )
| A. | 浓硫酸 | B. | 四氧化三铁 | C. | 氯化钠 | D. | 氢氧化钠 |
6.将一定量的乙醇和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如表,下列判断正确的是( )
| 物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
| A. | 表中a的值为2.6 | |
| B. | X中两种元素的质量比是3:8 | |
| C. | X可能含有氢元素 | |
| D. | 若起始时氧气的质量是9.6g,则无X生成 |