题目内容
向Fe(NO3)2、Mg(NO3)2和Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤.下列关于得到的溶液或滤渣的叙述正确的是(不考虑溶液中存在微量H+和OH-)( )
| A、若滤液中含有Fe2+,则滤渣中一定不含Fe |
| B、若滤渣中含Cu,则滤液中一定含Fe2+ |
| C、若滤渣中含Zn,则滤液中含2种离子 |
| D、若滤渣中不含Zn,则滤液中至少含3种离子 |
考点:金属的化学性质
专题:金属与金属材料
分析:根据已有的知识进行分析,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此解答.
解答:解:在Fe(NO3)2、Mg(NO3)2和Cu(NO3)2的混合溶液中加入一定量的锌粉,则锌能与硝酸铜和硝酸亚铁反应,
A、若滤液中含有Fe2+,则滤渣中可能含有Fe,此时加入锌粉能将全部的铜置换出来,并且和部分硝酸亚铁反应,故A错误;
B、加入的锌粉先和硝酸铜反应,故滤渣中一定含有Cu,滤液中不一定含Fe2+,此时若是加入的锌粉与全部的硝酸铜和硝酸亚铁反应,则滤液中不含有Fe2+,故B错误;
C、若滤渣中含Zn,则此时硝酸铜和硝酸亚铁全部参加反应,滤液中不含有铜离子和亚铁离子,只含有锌离子和镁离子,还含有硝酸根离子,故滤液中含2种离子是错误的;
D、若滤渣中不含Zn,则滤液中一定含有硝酸锌和硝酸镁,含有锌离子、镁离子、硝酸根离子,至少含3种离子,故D正确;
故选D.
A、若滤液中含有Fe2+,则滤渣中可能含有Fe,此时加入锌粉能将全部的铜置换出来,并且和部分硝酸亚铁反应,故A错误;
B、加入的锌粉先和硝酸铜反应,故滤渣中一定含有Cu,滤液中不一定含Fe2+,此时若是加入的锌粉与全部的硝酸铜和硝酸亚铁反应,则滤液中不含有Fe2+,故B错误;
C、若滤渣中含Zn,则此时硝酸铜和硝酸亚铁全部参加反应,滤液中不含有铜离子和亚铁离子,只含有锌离子和镁离子,还含有硝酸根离子,故滤液中含2种离子是错误的;
D、若滤渣中不含Zn,则滤液中一定含有硝酸锌和硝酸镁,含有锌离子、镁离子、硝酸根离子,至少含3种离子,故D正确;
故选D.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序结合其意义进行.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列实验操作正确的是( )
A、 过滤 |
B、 称量固体 |
C、 稀释浓硫酸 |
D、 测定液体的pH |
空气成分中,体积分数最大的是( )
| A、氮气 | B、氧气 |
| C、稀有气体 | D、水蒸气 |
 如图:是几种盐的溶解度曲线.下列说法正确的是( )
如图:是几种盐的溶解度曲线.下列说法正确的是( )| A、40℃时,将35g食盐溶于100g水中,降温至0℃时,可析出氯化钠晶体 |
| B、20℃时,硝酸钾饱和溶液的质量分数是31.6% |
| C、60℃时,200g水中溶解80g硫酸铜达饱和.当降温至30℃时,可析出30g硫酸铜晶体(即CuSO4?5H2O) |
| D、30℃时,将35g硝酸钾和35g食盐同时溶于100g水中,蒸发时先析出的是氯化钠晶体 |
下列说法错误的是( )
| A、利用洗洁精的乳化作用可以洗去餐具上的油污 |
| B、明矾既能净水又能杀菌消毒 |
| C、误食重金属盐,可立即服用蛋清或牛奶解毒 |
| D、蛋白质、糖类、油脂、维生素等是人体必需的营养素,但应注意膳食平衡 |
温度不变时,向烧杯中加入一定量水,仅有部分晶体溶解.下列说法正确的是( )
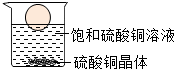

| A、溶液质量增加,溶液蓝色不变 |
| B、物质溶解度不变,塑料球下沉 |
| C、溶质质量增加,溶液浓度变大 |
| D、溶剂质量增加,变为不饱和溶液 |