题目内容
20.胃酸灵是一种医用药品,主要成分是碳酸镁和氢氧化铝,当胃酸(主要成分为盐酸)过多时,服用该药片后,在胃中可能发生的化学反应为(用化学方程式表示):①MgCO3+2HCl=MgCl2+H2O+CO2↑;
②Al(OH)3+3HCl═AlCl3+3H2O.
分析 碳酸镁与盐酸反应生成氯化镁、水和二氧化碳,氢氧化铝与盐酸反应生成氯化铝和水,写出反应的化学方程式即可.
解答 解:碳酸镁与盐酸反应生成氯化镁、水和二氧化碳,氢氧化铝与盐酸反应生成氯化铝和水,反应的化学方程式分别是MgCO3+2HCl=MgCl2+H2O+CO2↑、Al(OH)3+3HCl═AlCl3+3H2O.
故答案为:MgCO3+2HCl=MgCl2+H2O+CO2↑;Al(OH)3+3HCl═AlCl3+3H2O.
点评 本题难度不大,掌握酸的化学性质、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
相关题目
15.某同学进行实验探究时,欲配制10%的Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2试剂.在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在未溶物.为探究原因,该同学查得Ba(OH)2在20℃时的溶解度2.1g.
(1)烧杯中未溶物仅为BaCO3,理由是Ba(OH)2+CO2═BaCO3↓+H2O(用化学方程式表示).
(2)假设试剂由大量Ba(OH)2和少量BaCO3组成,设计实验方案,进行成分检验,在表格中写出实验步骤、预期现象和结论.
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、CuCl2溶液、烧杯、试管、带塞导气管、滴管.
(3)在20℃室温下,不能(选填“能”或“不能”)配制10%的Ba(OH)2溶液.
(1)烧杯中未溶物仅为BaCO3,理由是Ba(OH)2+CO2═BaCO3↓+H2O(用化学方程式表示).
(2)假设试剂由大量Ba(OH)2和少量BaCO3组成,设计实验方案,进行成分检验,在表格中写出实验步骤、预期现象和结论.
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、CuCl2溶液、烧杯、试管、带塞导气管、滴管.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀. | |
步骤2:取适量滤液于试管中,滴加稀硫酸. | 有①生成,说明有Ba2+. |
| 步骤3:取适量步骤1中的沉淀于试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中. | 试管中有②产生,烧杯中 ③,结合步骤2说明沉淀是BaCO3. |
| 步骤4:取适量滤液于试管中,滴加④. | 试管中有蓝色沉淀生成,说明滤液中有大量的OH-,综合上面步骤可知试剂由大量Ba(OH)2和少量BaCO3组成,假设成立. |
4.下列物质名称和俗称对应正确的是( )
| A. | 碳酸钙-纯 碱 | B. | 氯化钠-食 盐 | C. | 碳酸钠-小苏打 | D. | 氧化钙-熟石灰 |
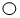 ”代表氢原子,“
”代表氢原子,“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子).
”代表氧原子).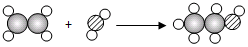
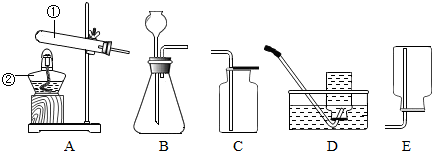
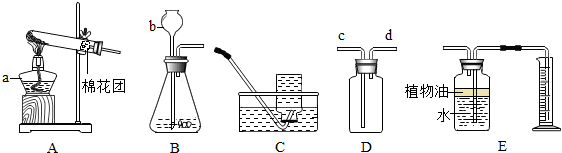
 (1)如图所示,将二氧化碳倒入烧杯中.现象:烧杯中的蜡烛下面的先熄灭,上面的后熄灭;
(1)如图所示,将二氧化碳倒入烧杯中.现象:烧杯中的蜡烛下面的先熄灭,上面的后熄灭;