题目内容
18.为了制取CO2并验证它的性质,张林同学设计并进行了如图所示的实验,请根据要求回答有关问题.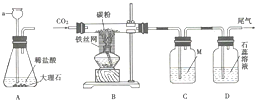
(1)仪器a的名称是长颈漏斗,A装置的突出优点是控制化学反应速率,A中发生反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)B中玻璃管内发生化学反应的方程式为C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO,酒精灯加上铁丝网罩的作用是使火集中并提高温度.
(3)尾气的处理方法可以是点燃.
分析 (1)认识常见化学仪器;根据反应原理来书写化学方程式;
(2)根据反应原理来书写化学方程式;根据酒精灯火焰加上网罩后火焰集中分析解答;
(3)根据尾气中含有一氧化碳来分析.
解答 解:
(1)根据图可知:仪器a的名称是长颈漏斗,A装置的突出优点是控制化学反应速率,A中发生反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)根据图可知:B中玻璃管内发生化学反应的方程式为C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO,酒精灯加上铁丝网罩的作用是使火集中并提高温度.
(3)因为尾气中含有一氧化碳,一氧化碳有毒,故尾气的处理方法可以是点燃.
故答案为:
(1)长颈漏斗; 控制化学反应速率; CaCO3+2HCl═CaCl2+H2O+CO2↑;(2)C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO,使火集中并提高温度;(3)点燃(或收集).
点评 此题通过实验,巧妙的把二氧化碳的实验室制法和性质、一氧化碳的性质融合在一起,有较强的综合性.对于化学方程式的书写,可以联系着质量守恒定律、元素符号和化学式的书写及其意义、化学方程式的配平、常见物质的状态等相关知识细心地进行书写.

练习册系列答案
相关题目
11.等质量的氢气、甲烷和一氧化碳完全燃烧需要氧气的质量( )
| A. | CO最多,H2最少 | B. | H2最多,CH4最少 | C. | H2最多,CO最少 | D. | CH4最多,CO最少 |
13.有一种石灰石样品,其中含有的杂质是二氧化硅(二氧化硅是一种不溶于水、不与酸反应、耐高温的固体),某学生想测定该样品的纯度,他取用2g这种石灰石样品,把15g盐酸分三次加入,充分反应后剩余固体质量见表:
求:
(1)石灰石样品的纯度是多少?
(2)100Kg这种纯度的石灰石充分煅烧分解后可以得到的固体质量是多少Kg?
(3)该同学所使用的盐酸的质量分数是多少(小数点后保留两位)?
| 稀盐酸的用量 | 剩余固体的质量 |
| 第1次加入5g | 1.3g |
| 第2次加入5g | 0.6g |
| 第3次加入5g | 0.2g |
(1)石灰石样品的纯度是多少?
(2)100Kg这种纯度的石灰石充分煅烧分解后可以得到的固体质量是多少Kg?
(3)该同学所使用的盐酸的质量分数是多少(小数点后保留两位)?
3.下列过程中发生了化学变化的是( )
| A. | 海水晒盐 | B. | 麻线织布 | C. | 牛奶变酸 | D. | 浓盐酸挥发 |
10.春季是由病毒引起的流感的高发季节.下面是自来水消毒过程中发生反应的微观图,产物之一是次氯酸(HClO),起到杀菌消毒作用.下列说法错误的是( )


| A. | 此反应为分解反应 | B. | 反应遵守质量守恒定律 | ||
| C. | 图中共有四种分子 | D. | 该反应中氯元素的化合价发生改变 |
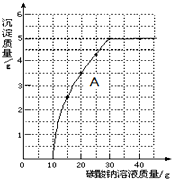 实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题:
实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题: