题目内容
11.等质量的氢气、甲烷和一氧化碳完全燃烧需要氧气的质量( )| A. | CO最多,H2最少 | B. | H2最多,CH4最少 | C. | H2最多,CO最少 | D. | CH4最多,CO最少 |
分析 根据氢气和氧气反应会生成水,甲烷和氧气反应生成水和二氧化碳,一氧化碳和氧气反应生成二氧化碳,可以假设参加反应的氢气、甲烷和一氧化碳的质量是1g,然后依据化学方程式求出需要的氧气的质量,再比较大小.
解答 解:解:设参加反应的氢气、甲烷和一氧化碳的质量是1g,需要的氧气的质量分别是x,y,z,所以
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2
4 32 16 64 56 32
1g x 1g y 1g z
$\frac{4}{32}=\frac{1g}{x}$ $\frac{16}{64}=\frac{1g}{y}$ $\frac{56}{32}=\frac{1g}{z}$
x=8g y=4g z=$\frac{4}{7}$g
故H2最多,CO最少,故选C
点评 本题主要考查了利用化学方程式进行计算,可以采用假设法,然后结合各物质之间的反应关系进行解答.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目
2.下列物质所含的主要材料中属于合成材料的是( )
| A. | 真丝围巾 | B. | 不锈钢水壶 | C. | 玻璃杯 | D. | 塑料桶 |
19.下列图示操作中正确的是( )
| A. | 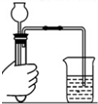 检查装置气密性 | B. | 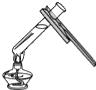 加热液体 | C. | 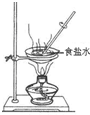 蒸发结晶 | D. |  称量 |
20.分析推理是化学学习常用的方法,下列分析推理正确的是( )
| A. | 单质中只含有一种元素,因此只含有一种元素的物质一定是单质 | |
| B. | 金刚石和石墨都是由碳原子构成,所以它们的性质相同 | |
| C. | 离子是带电荷的粒子,所以带电荷的粒子一定是离子 | |
| D. | 点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度 |
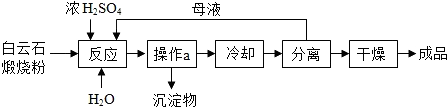
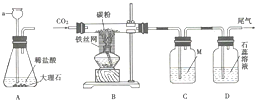
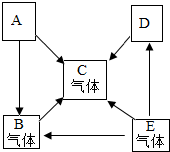 已知A、B、C、D、E是初中化学中常见的五种物质,其中A、D是黑色固体,B、C、E是无色气体,B的相对分子质量小于气体C,化合物D中含有铁元素,它们在一定条件下的转化关系如图所示(→表示转化),请回答下列问题:
已知A、B、C、D、E是初中化学中常见的五种物质,其中A、D是黑色固体,B、C、E是无色气体,B的相对分子质量小于气体C,化合物D中含有铁元素,它们在一定条件下的转化关系如图所示(→表示转化),请回答下列问题: