题目内容
13.氧气是我们生存的必需物质,它对我们的生活有着至关重要的影响.某化学实验小组在实验室用分解氯酸钾的方法制氧气.他们取来100g氯酸钾和二氧化锰的混合物,并按规范的操作方法进行操作.当实验结束后,试管中剩余物质的质量为61.6g,求:(1)实验结束后,该小组制得的氧气的质量共计38.4g.
(2)实验小组用于实验的混合物中,二氧化锰的质量分数.
分析 反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算氯酸钾的质量,进一步可以计算二氧化锰的质量以及质量分数.
解答 (1)根据题意得,实验结束后,该小组制得的氧气的质量共计100.0g-61.6g=38.4g,故填:38.4,
(2)设参加反应的KClO3的质量为x.
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 96
x 38.4g
$\frac{245}{x}=\frac{96}{38.4g}$
x=98g
混合物中二氧化锰的质量分数为$\frac{100g-98g}{100g}×100%$=2%.
答:混合物中二氧化锰的质量分数为2%.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
3.下列叙述完全正确的是( )
| A. | 碳酸钠溶液能使无色酚酞试液变红 | |
| B. | 过氧化氢是由氢原子和氧原子构成的,它与水的组成元素相同 | |
| C. | 某白色固体与熟石灰混合后加热,产生可使湿润的红色石蕊试纸变蓝的气体,证明该固体是铵盐 | |
| D. | 分子都是由不同原子构成的 |
1.铜锌合金是一种记忆合金,俗称黄铜.张炎同学想要测定铜锌合金的组成(假设只有铜、锌两种元素),便进行了如下实验操作:将42g铜锌合金放入烧杯中后,又将219g稀盐酸分3次加入盛有铜锌合金的烧杯中;每次充分反应后,测得烧杯内固体减少的质量如下表所示.求:(忽略操作过程中溶液的损失)
(1)铜锌合金中铜的质量为27g.
(2)实验所用的稀盐酸的溶质质量分数.
| 次数 | 1 | 2 | 3 |
| 加入稀盐酸的质量/g | 73 | 73 | 73 |
| 固体减少的质量/g | 6.5 | 6.5 | 2 |
(2)实验所用的稀盐酸的溶质质量分数.
8.请你根据如图所示的溶解度曲线判断,下列说法中正确的是( )
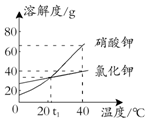

| A. | 氯化钾在20℃时的溶解度比硝酸钾大 | |
| B. | 将40℃的硝酸钾溶液降温至20℃,溶液中一定会有晶体析出 | |
| C. | 将等量的氯化钾和硝酸钾分别放于等量的水中,把温度调为t1℃,此时,二者的溶质质量分数相等 | |
| D. | 当温度高于t1℃时,饱和硝酸钾的溶剂质量分数比饱和氯化钾的大 |
18.下列关于物质的性质或变化叙述正确的是( )
| A. | 活性炭净水--化学性质 | |
| B. | 盐酸使石蕊溶液变红--物理性质 | |
| C. | 冰川融化--物理变化 | |
| D. | 工业上分离液态空气制取氧气、氮气--化学变化 |
5.潜水艇出航时贮备的“过氧化钠”(Na2O2)是一种淡黄色固体,吸收二氧化碳后变为纯碱并释放出氧气,它是艇员呼吸时理想的供氧剂,以上叙述没有涉及过氧化钠 ( )
| A. | 制法 | B. | 用途 | C. | 物理性质 | D. | 化学性质 |
3.进行下列对比试验,不需要控制变量的是( )
| A. | 用氯化钙溶液检验某氢氧化钠溶液是否变质 | |
| B. | 用红磷和白磷探究可燃物燃烧的条件 | |
| C. | 用铁钉探究铁生锈的条件 | |
| D. | 用镁、锌与稀硫酸反应,比较镁、锌的金属活动性强弱 |
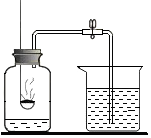 某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格.
某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格.