题目内容
6.在101.8g硫酸铜溶液中加入一定质量的氢氧化钠溶液,恰好完全反应,共得到9.8g沉淀和溶质质量分数为10%的反应后的溶液.(反应的化学方程式为:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4 )求:(1)参加反应的硫酸铜的质量.
(2)所加入的氢氧化钠溶液中溶质的质量分数.
分析 根据氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,依据题中的数据计算参加反应的硫酸铜的质量和参加反应的氢氧化钠的质量,然后计算氢氧化钠的质量分数.
解答 解:设参加反应的氢氧化钠的质量为x,硫酸铜的质量为y,生成硫酸钠的质量为z
CuSO4+2NaOH═Cu(OH)2↓+Na2SO4,
160 80 98 142
y x 9.8g z
$\frac{160}{y}$=$\frac{80}{x}$=$\frac{98}{9.8g}$=$\frac{142}{z}$
x=8g
y=16g
z=14.2g
所以反应后硫酸钠溶液的质量为:$\frac{14.2g}{10%}$=142g,
所以氢氧化钠溶液的质量为:142g+9.8g-101.8g=50g,所以氢氧化钠溶液的质量分数为:$\frac{8g}{50g}$×100%=16%.
故答案为:(1)16g;
(2)16%.
点评 不同主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
17.下列液态物质中,不属于溶液的是( )
| A. | 食盐水 | B. | 碘酒 | C. | 液氢 | D. | 矿泉水 |
11.把含镁元素质量相等的下列物质,投入足量且等质量的稀盐酸中充分反应后,所得溶液中的MgCl2质量分数最小的是( )
| A. | Mg(OH)2 | B. | MgO | C. | Mg | D. | MgCO3 |
18.下列有关量的变化图象与其对应叙述相符的是( )
| A. | 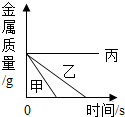 向三份完全相同稀盐酸中分别加入甲、乙、丙三种金属、则金属活动性顺序为丙>乙>甲 向三份完全相同稀盐酸中分别加入甲、乙、丙三种金属、则金属活动性顺序为丙>乙>甲 | |
| B. |  t℃时,向等质量的甲、乙、丙三种物质中分别加水配成饱和溶液,所得溶液质量最大的是甲 t℃时,向等质量的甲、乙、丙三种物质中分别加水配成饱和溶液,所得溶液质量最大的是甲 | |
| C. |  金属与相同质量相同质量分数的稀硫酸反应,若金属M与N在化合和中化合价都为+2,则相对原子质量M>N 金属与相同质量相同质量分数的稀硫酸反应,若金属M与N在化合和中化合价都为+2,则相对原子质量M>N | |
| D. |  向氯化钠饱和溶液中加入硫酸钾 向氯化钠饱和溶液中加入硫酸钾 |
16. 如图是实验室制取氧气时,各物质的质量随加热时间的变化关系,下列叙述正确的是( )
如图是实验室制取氧气时,各物质的质量随加热时间的变化关系,下列叙述正确的是( )
 如图是实验室制取氧气时,各物质的质量随加热时间的变化关系,下列叙述正确的是( )
如图是实验室制取氧气时,各物质的质量随加热时间的变化关系,下列叙述正确的是( )| A. | ①表示反应物高锰酸钾 | B. | ②表示催化剂 | ||
| C. | ③表示生成物氧气 | D. | ④表示反应物氯酸钾 |




