题目内容
6.如图所示实验能达到目的是( )| A. |  分离溶液中NaCl和KNO3两种溶质 | B. |  检验蜡烛中是否含有氧元素 | ||
| C. |  用水吸收CO | D. |  探究燃烧的条件 |
分析 A、根据氯化钠和硝酸钾均易溶于水,进行分析判断.
B、根据质量守恒定律,反应前后元素种类不变,进行分析判断.
C、根据一氧化碳难溶于水,不与水反应,进行分析判断.
D、根据薄铜片上的白磷和红磷、水中的白磷的燃烧情况,进行分析判断.
解答 解:A、氯化钠和硝酸钾均易溶于水,用过滤的方法不能进行分离,故选项实验不能达到目的.
B、干冷的烧杯能检验是否有水生成,图中现象是烧杯内壁上出现水雾,说明生成了水;H2O中含有氢、氧元素,根据质量守恒定律,反应前后,元素种类不变,反应物氧气中只含有氧元素,则蜡烛中一定含有氢元素,可能含有氧元素,故选项实验不能达到目的.
C、一氧化碳难溶于水,不与水反应,不能用水吸收一氧化碳,故选项实验不能达到目的.
D、铜片的白磷燃烧,红磷不燃烧,水中的白磷不能燃烧,薄铜片上的白磷能与氧气接触,温度能达到着火点,水中的白磷不能与氧气接触,红磷温度没有达到着火点;可得出燃烧需要与氧气接触,且温度达到着火点,故选项实验能达到目的.
故选:D.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体解题时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
17.下列图示实验操作中,正确的是(氢氧化钠化学式NaOH,易潮解,强腐蚀)( )
| A. | 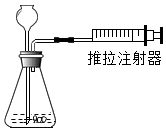 检查装置气密性 | B. |  滴加试剂 | ||
| C. | 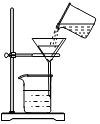 过滤 | D. | 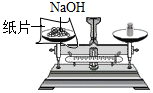 称量氢氧化钠 称量氢氧化钠 |
18.下列实验现象描述不正确的是( )
| A. | 将二氧化碳通入紫色石蕊溶液中,溶液变红 | |
| B. | 铁丝在氧气中剧烈燃烧,火星四射 | |
| C. | 红磷在空气中燃烧,产生大量白烟 | |
| D. | 硫在氧气中燃烧,火焰呈淡蓝色 |
15.向饱和氢氧化钙溶液中加入少量氧化钙固体,充分反应后恢复到原温度,则下列说法正确的是( )
| A. | 反应后溶液质量变大 | B. | 反应后溶剂质量不变 | ||
| C. | 反应后溶质质量变大 | D. | 反应后溶质质量分数不变 |
16.在化学反应A+B═C+D 中,6克A 与8克B 恰好完全反应,生成9克D.则生成C 的质量为( )
| A. | 6克 | B. | 8克 | C. | 5克 | D. | 9克 |
 如图所示是电解水的简易装置:
如图所示是电解水的简易装置: 化学与社会、人们的生活密切相关,请根据下列要求回答问题.
化学与社会、人们的生活密切相关,请根据下列要求回答问题.