题目内容
16.下列叙述中,正确的是( )| A. | 氢原子结合形成氢气 | |
| B. | 物质在不同条件下的三态变化主要是由于分子的大小发生了变化 | |
| C. | 气体易被压缩,说明构成气体的分子在不断运动 | |
| D. | 原子的质量主要集中在原子核上 |
分析 A、氢气是由氢分子构成的去分析;
B、物质的三态变化主要取决于分子间间隔的大小去分析;
C、从气体容易被压缩,说明构成气体的分子之间有间隔去分析;
D、从原子的质量主要集中在原子核上去分析.
解答 解:A、氢气是由氢分子构成的;故错误;
B、物质在不同条件下的三态变化主要是由于分子间间隔的大小发生了变化;故错误;
C、气体容易被压缩,说明构成气体的分子之间有间隔;故错误;
D、由于电子的质量很小,每个电子的质量大约是每个质子质量的1/1836,因此原子的质量主要集中在原子核上;故正确;
故答案为:D.
点评 本题难度不大,掌握分子的原子的基本性质是正确解答本题的关键.

练习册系列答案
相关题目
6. 分类法是学习化学的重要思想方法.
分类法是学习化学的重要思想方法.
(1)人们可以对物质从不同的角度进行分类.请根据示例将酒精、醋酸、水、食盐四种物质进行分类,
并写出分类依据.
(2)某同学从物质类别的角度构建了如“图一”所示的知识网络图,借助网络图回答:
①写出用酸和碱生成氯化钠的化学方程式NaOH+HCl=NaCl+H2O.
②请把如图中①处补充完整,要求不能与图中已有信息重复.则①处应填写的内容是盐+金属.
③铁的金属活动性比铜强(选填:“强”或“弱”).可证明该结论的化学方程式是Fe+CuSO4=FeSO4+Cu.
 分类法是学习化学的重要思想方法.
分类法是学习化学的重要思想方法.(1)人们可以对物质从不同的角度进行分类.请根据示例将酒精、醋酸、水、食盐四种物质进行分类,
并写出分类依据.
| 不同类的物质 | 分类依据 | |
| 示例 | 水 | 水是氧化物,其余不是氧化物 |
| 分类一 | 食盐 | 常温下食盐是固体,其余是液体 |
| 分类二 | 醋酸 | 醋酸是酸,其余的不是酸 |
①写出用酸和碱生成氯化钠的化学方程式NaOH+HCl=NaCl+H2O.
②请把如图中①处补充完整,要求不能与图中已有信息重复.则①处应填写的内容是盐+金属.
③铁的金属活动性比铜强(选填:“强”或“弱”).可证明该结论的化学方程式是Fe+CuSO4=FeSO4+Cu.
11.南京大学邹志刚课题组及其合作者利用ZnGa2O4介孔光催化材料用于CO2的光还原,成功地实现了将CO2转化为碳氢化合物燃料.该反应化学方程式为 CO2+2H2O$\frac{\underline{\;ZnGa_{2}O_{4}\;}}{\;}$CH4+2O2.下列有关该反应说法错误的是
( )
( )
| A. | 此反应为CO2的利用创造一种新的方法 | |
| B. | 此反应前后分子个数不变 | |
| C. | 此反应属于置换反应 | |
| D. | 此反应制取的CH4可以再利用 |
8.常用于实验室制取氧气的高锰酸钾(KMnO4)属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
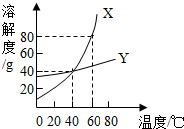 X、Y两种固体物质的溶解度曲线如图所示.回答下列问题:
X、Y两种固体物质的溶解度曲线如图所示.回答下列问题:
 如图所示,老师在演示用过氧化氢和二氧化锰制取氧气的实验中,收集完氧气后,反应还在继续进行.小明同学认为,这个装置的缺点是不能控制反应随时发生、随时停止,造成了药品的浪费.
如图所示,老师在演示用过氧化氢和二氧化锰制取氧气的实验中,收集完氧气后,反应还在继续进行.小明同学认为,这个装置的缺点是不能控制反应随时发生、随时停止,造成了药品的浪费.