题目内容
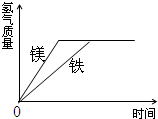 有等质量的镁和铁,二者都放入质量分数为10%的稀硫酸中,产生氢气的质量随时间变化曲线如图所示.下列说法错误的是( )
有等质量的镁和铁,二者都放入质量分数为10%的稀硫酸中,产生氢气的质量随时间变化曲线如图所示.下列说法错误的是( )| A、镁和铁中至少有一种剩余 |
| B、消耗的稀硫酸质量相等 |
| C、若只有一种金属剩余一定是铁剩余 |
| D、产生氢气的质量相等 |
考点:金属的化学性质
专题:金属与金属材料
分析:本题通过图象分析得出二者生成氢气的质量相等,给出一个方便计算的特殊数值,例如氢气的相对分子质量为2,可设制取2g氢气,然后分别计算所需镁、铁、稀硫酸、稀盐酸的质量,便可得出答案.
解答:解:设制取2g氢气需要镁的质量为x,设制取2g氢气需要铁的质量为x,
需稀硫酸的质量为z; 需稀硫酸的质量为m
Mg+H2SO4═MgSO4+H2↑; Fe+H2SO4═FeSO4+H2↑
24 98 2 56 98 2
x z×10% 2g y m×10% 2g
则
=
=
;
=
=
,解之得:x=24g; z=980g y=56g; m=980g
由上面的计算可知:要想制取相同质量的氢气(2g),需要镁的质量是24g,而需要铁的质量为56g.而题目中指出是相同质量的金属,假设制取2g氢气,需56g铁,因此镁的质量也是56g故镁有剩余:56g-24g=32g,故A、B、D的说法是正确的.
故选:C.
需稀硫酸的质量为z; 需稀硫酸的质量为m
Mg+H2SO4═MgSO4+H2↑; Fe+H2SO4═FeSO4+H2↑
24 98 2 56 98 2
x z×10% 2g y m×10% 2g
则
| 24 |
| x |
| 98 |
| z×10% |
| 2 |
| 2g |
| 56 |
| y |
| 98 |
| m×10% |
| 2 |
| 2g |
由上面的计算可知:要想制取相同质量的氢气(2g),需要镁的质量是24g,而需要铁的质量为56g.而题目中指出是相同质量的金属,假设制取2g氢气,需56g铁,因此镁的质量也是56g故镁有剩余:56g-24g=32g,故A、B、D的说法是正确的.
故选:C.
点评:题目中没有给出具体的数据,这类题目可以给出一个方便计算的特殊数值,例如物质的相对分子质量等.

练习册系列答案
相关题目
水是生命之源,下列有关水的说法错误的是( )
| A、通过过滤可以除去水中所有的杂质 |
| B、用肥皂水可以区分硬水和软水 |
| C、生活中可以用煮沸的方法降低水的硬度 |
| D、水是一种重要的溶剂 |
吸烟有害健康,在公共场所吸烟会使周围的人被动地吸“二手烟”.“二手烟”中含有一种能与人体血液中血红蛋白结合的有毒气体,该气体是( )
| A、氮气 | B、氧气 |
| C、二氧化碳 | D、一氧化碳 |
用H2、木炭粉、CO作还原剂分别与质量相同的CuO在高温下反应,消耗H2、C、CO三种物质的质量比为( )
| A、1:1:1 |
| B、1:3:14 |
| C、1:6:14 |
| D、2:1:2 |
下列反应既不是化合反应,也不是分解反应,但属于氧化反应的是( )
A、铝+氧气
| ||
| B、二氧化碳+水→碳酸 | ||
C、甲烷+氧气
| ||
D、水
|
下列应用的原理用化学方程式表示正确的是( )
| A、用电解水的方法测定水的组成:2H2O=O2+2H2 |
| B、用氢氧化钠溶液吸收二氧化碳:2NaOH+CO2=Na2CO3+H2O |
| C、用小苏打治疗胃酸过多:Na2CO3+2HCl=2NaCl+H2O+CO2 |
| D、用石灰石制取生石灰:CaCO3=CaO+CO2 |