题目内容
无标签试剂瓶中的一种黑色不溶于水的固体可能是硫化铜或者是硫化亚铜.查资料可知:硫化铜(CuS)和硫化亚铜(Cu2S)在空气中灼烧分别发生下列化学反应:
2CuS+3O2
2CuO+2SO2 Cu2S+O2
CuO+SO2(没配平)
(1)请写出配平后的Cu2S在空气中灼烧的化学方程式 .如要确定灼烧的Cu2S是否完全反应,依据的实验现象是 .
(2)根据这两个反应的化学方程式中固体物质的质量变化,某同学仅用天平、酒精灯、坩埚、三角架等常用仪器(无其它试剂),通过三个实验步骤鉴别出某黑色固体是硫化铜还是硫化亚铜.他的实验步骤一:用天平准确称量一定质量的待测黑色固体.
请写出后两个实验步骤:
实验步骤二:
实验步骤三: .
2CuS+3O2
| ||
| ||
(1)请写出配平后的Cu2S在空气中灼烧的化学方程式
(2)根据这两个反应的化学方程式中固体物质的质量变化,某同学仅用天平、酒精灯、坩埚、三角架等常用仪器(无其它试剂),通过三个实验步骤鉴别出某黑色固体是硫化铜还是硫化亚铜.他的实验步骤一:用天平准确称量一定质量的待测黑色固体.
请写出后两个实验步骤:
实验步骤二:
实验步骤三:
考点:物质的鉴别、推断
专题:物质的检验、鉴别与推断
分析:(1)依据质量守恒定率进行配平;根据Cu2S燃烧生成的SO2,通过SO2的性质作出判断,即可确定灼烧的Cu2S是否完全反应;
(2)根据CuS燃烧后固体质量减小.而Cu2S燃烧后固体质量不变的原理.
(2)根据CuS燃烧后固体质量减小.而Cu2S燃烧后固体质量不变的原理.
解答:解:(1)依据质量守恒定率,Cu2S在空气中灼烧的化学方程式为:Cu2S+2O2
2CuO+SO2;根据Cu2S燃烧生成的SO2,的性质作出判断,所以不再产生刺激性气味的气体,或将湿润的蓝色石蕊试纸悬于灼烧容器上方,试纸不变色都可以确定灼烧的Cu2S是否完全反应;
(2)由化学方程式,2CuS+3O2
2CuO+2SO2 △m,Cu2S+2O2
2CuO+SO2 △m,
192 160 32 160 160 0
可以看出CuS燃烧后固体质量减小,而Cu2S燃烧后固体质量不变,因此可通过固体燃烧前后的质量差进行鉴别,写出实验步骤2:将称量好的黑色固体分别置于坩埚中充分灼烧,步骤3:冷却至室温后称量其剩余固体的质量,即可判断黑色固体是硫化铜还是硫化亚铜.
故答案为:(1)Cu2S+2O2
2CuO+SO2;
不再产生刺激性气味的气体或将湿润的蓝色石蕊试纸悬于灼烧容器上方,试纸不变色;
(2)将称量好的黑色固体分别置于坩埚中充分灼烧;
冷却至室温后称量其剩余固体的质量.
| ||
(2)由化学方程式,2CuS+3O2
| ||
| ||
192 160 32 160 160 0
可以看出CuS燃烧后固体质量减小,而Cu2S燃烧后固体质量不变,因此可通过固体燃烧前后的质量差进行鉴别,写出实验步骤2:将称量好的黑色固体分别置于坩埚中充分灼烧,步骤3:冷却至室温后称量其剩余固体的质量,即可判断黑色固体是硫化铜还是硫化亚铜.
故答案为:(1)Cu2S+2O2
| ||
不再产生刺激性气味的气体或将湿润的蓝色石蕊试纸悬于灼烧容器上方,试纸不变色;
(2)将称量好的黑色固体分别置于坩埚中充分灼烧;
冷却至室温后称量其剩余固体的质量.
点评:本题主要考查化学方程式的配平以及质量守恒定律的运用,以及SO2的性质,难度较大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
利用如图所示实验不能实现的探究目的是 ( )
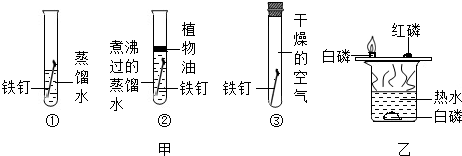

| A、甲可探究铁的锈蚀与植物油是否有关 |
| B、甲可探究铁的锈蚀与水是否有关 |
| C、乙可探究可燃物的燃烧是否需要达到一定温度 |
| D、乙可探究可燃物的燃烧是否需要与氧气接触 |
下列属于物理变化的是( )
| A、镁带变黑 | B、干冰升华 |
| C、牛奶变酸 | D、铝箔发暗 |
 如图是实验室常用的制取气体的装置
如图是实验室常用的制取气体的装置