题目内容
3.从含有AgNO3和Cu(NO3)2的废液中回收金属银和铜,设计的生产方案如图所示:
(1)加入的X、Y分别是铜、铁
(2)写出②③两步反应的化学方程式:②Fe+Cu(NO3)2═Fe(NO3)2+Cu ③Fe+H2SO4═FeSO4+H2↑.
分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能间位于其后的金属从其盐溶液中置换出来,在硝酸铜和硝酸银的混合溶液中加入X的到的是银和硝酸铜溶液,则X为铜,在硝酸铜溶液中加入Y得到了硝酸亚铁溶液和铜与铁的混合物,则Y是铁,铁能与硫酸反应生成硫酸亚铁和氢气.
解答 解:(1)在硝酸铜和硝酸银的混合溶液中加入X的到的是银和硝酸铜溶液,则X为铜,在硝酸铜溶液中加入Y得到了硝酸亚铁溶液和铜与铁的混合物,则Y是铁,铁能与硫酸反应生成硫酸亚铁和氢气,所以答案为:铜,铁.
(2)根据分析,结合图框,铁能与硝酸铜反应生成硝酸亚铁和铜,铁能与硫酸反应生成硫酸亚铁和氢气,所以其反应的化学方程式为:Fe+Cu(NO3)2═Fe(NO3)2+Cu,Fe+H2SO4═FeSO4+H2↑.
故答案为:
(1)铜、铁;(2)Fe+Cu(NO3)2═Fe(NO3)2+Cu; Fe+H2SO4═FeSO4+H2↑.
点评 本题是一道推断题,要求学生能根据图表中的内容,恰当的选出所需要的物质,完成此题可以依据金属活动性顺序及其意义进行,考查了学生的综合能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
14.某班同学在实验室制取二氧化碳,老师观察到了四个同学的如下操作,其中正确的是( )
| A. | 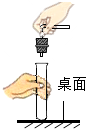 连接仪器 | B. | 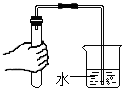 检查气密性 | C. |  量筒读数 | D. |  CO2验满 |


 化学活动课上,老师给同学们表演了一个“水能生火”的魔术(如图所示),他将包有过氧化钠(Na2O2)粉末的脱脂棉放在石棉网上,向脱脂棉上滴了几滴水,脱脂棉立刻燃烧起来.通过查阅资料可知,过氧化钠和水反应的产物只有两种,都是初中化学常见的物质.根据所学化学知识回答:
化学活动课上,老师给同学们表演了一个“水能生火”的魔术(如图所示),他将包有过氧化钠(Na2O2)粉末的脱脂棉放在石棉网上,向脱脂棉上滴了几滴水,脱脂棉立刻燃烧起来.通过查阅资料可知,过氧化钠和水反应的产物只有两种,都是初中化学常见的物质.根据所学化学知识回答: