题目内容
2014 APCE之夜燃放环保烟花,减少了硫粉和金属粉末的使用,保护了环境.
(1)分离液化空气可获得氮气和 两种主要气体;氮气用作保护气,说明氮气 .
(2)利用膜分离技术,在一定压力下让空气通过具有富集氧气功能的薄膜,能得到含氧量较高的富氧空气,该过程发生 变化.
(3)实验室制取气体装置如图:
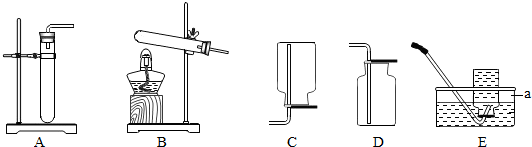
①图中仪器a的名称为 .
②实验室用过氧化氢制取氧气,应≤选用的发生装置是 (填字母序号),该反应化学方程式为 .
③若用B装置制备氧气,发生反应的化学方程式为 .
④若用E装置收集满氧气后,取出的集气瓶应 (填“正””或“倒”)放在实验台上.若用排气法收集氧气时,检验氧气是否收集满的方法是 .
⑤已知甲烷(CH4)气体难溶于水,密度小于空气.若要收集干燥的甲烷气体,应选用的装置是 .
(4)硫粉在空气中能燃烧,放出具有 气味的气体,产生 火焰,该反应的化学方程式为 反应类型 .
(5)铁粉在氧气中剧烈燃烧, ,放出大量的热,生成黑色固体.在实验室进行此实验时,集气瓶底部放少量水或沙子的目的是 .
(1)分离液化空气可获得氮气和
(2)利用膜分离技术,在一定压力下让空气通过具有富集氧气功能的薄膜,能得到含氧量较高的富氧空气,该过程发生
(3)实验室制取气体装置如图:

①图中仪器a的名称为
②实验室用过氧化氢制取氧气,应≤选用的发生装置是
③若用B装置制备氧气,发生反应的化学方程式为
④若用E装置收集满氧气后,取出的集气瓶应
⑤已知甲烷(CH4)气体难溶于水,密度小于空气.若要收集干燥的甲烷气体,应选用的装置是
(4)硫粉在空气中能燃烧,放出具有
(5)铁粉在氧气中剧烈燃烧,
考点:氧气的制取装置,氧气的化学性质,氧气的收集方法,氧气的检验和验满,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据分离液化空气可获得氮气和氧气,氮气化学性质不活泼,因此氮气可用作保护气;
(2)利用膜分离技术,在一定压力下让空气通过具有富集氧气功能的薄膜,能得到含氧量较高的富氧空气,该过程发生物理变化,因为没有新物质生成;
(3)
①根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
②根据实验室用过氧化氢溶液制取氧气的反应物是固体和液体,反应条件是常温,过氧化氢在二氧化锰的催化作用下分解生成水和氧气进行分析;
③根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
④根据氧气的密度比空气大,氧气有助燃性进行分析;
⑤根据甲烷难溶于水,密度小于空气进行分析;
(4)硫在空气中燃烧生成二氧化硫,产生淡蓝色火焰,而在氧气中燃烧,发出蓝紫色火焰;
(5)根据铁丝在氧气中燃烧的现象、注意事项等分析回答;
(2)利用膜分离技术,在一定压力下让空气通过具有富集氧气功能的薄膜,能得到含氧量较高的富氧空气,该过程发生物理变化,因为没有新物质生成;
(3)
①根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
②根据实验室用过氧化氢溶液制取氧气的反应物是固体和液体,反应条件是常温,过氧化氢在二氧化锰的催化作用下分解生成水和氧气进行分析;
③根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
④根据氧气的密度比空气大,氧气有助燃性进行分析;
⑤根据甲烷难溶于水,密度小于空气进行分析;
(4)硫在空气中燃烧生成二氧化硫,产生淡蓝色火焰,而在氧气中燃烧,发出蓝紫色火焰;
(5)根据铁丝在氧气中燃烧的现象、注意事项等分析回答;
解答:解:
(1)空气的成分主要以氮气和氧气为主,氧气约占五分之一,氮气约占五分之四,分离液化空气可获得氮气和氧气,氮气化学性质不活泼,因此氮气可用作保护气;故答案为:氧气;化学性质不活泼
(2)利用膜分离技术,在一定压力下让空气通过具有富集氧气功能的薄膜,能得到含氧量较高的富氧空气,该过程发生物理变化,因为没有新物质生成;故答案为:物理
(3)
①通过分析题中所指仪器的作用可知,a是水槽;
②实验室用过氧化氢溶液制取氧气的反应物是固体和液体,反应条件是常温,所以选用的发生装置是:A,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,反应的方程式是:2H2O2
2H2O+O2↑;
③用B装置制备氧气的反应物是固体,反应条件是加热,所以可以选用高锰酸钾,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的方程式是:2KMnO4
K2MnO4+MnO2+O2↑;
④氧气的密度比空气大,所以收集氧气后,取出的集气瓶应正放在实验台上,氧气有助燃性,所以检验氧气是否收集满的方法是:将带火星的木条放在集气瓶口,木条复燃,证明集满;
⑤甲烷难溶于水,密度小于空气,所以收集干燥的甲烷气体要用向下排空气法,选用的装置是:C.
(4)淡黄色的硫粉在空气中燃烧发出淡蓝色的火焰,而在氧气中燃烧,发出蓝紫色火焰,且生成无色有刺激性气味的气体,化学方程式为:S+O2
SO2.符合多变一,属于化合反应;
(5)铁丝在氧气中剧烈燃烧、火星四射、生成一种黑色固体;在集气瓶底部放少量的水,其目的是防止溅落的熔化物炸裂瓶底,故填:火星四射;防止溅落的熔化物炸裂瓶底;
答案:
(1)氧气;化学性质不活泼
(2)物理
(3)
①水槽;
②A 2H2O2
2H2O+O2↑
③2KMnO4
K2MnO4+MnO2+O2↑
④正,将带火星的木条放在集气瓶口,木条复燃,证明集满;
⑤C
(4)刺激性 淡蓝色 S+O2
SO2化合反应
(5)火星四射 防止溅落的熔化物炸裂瓶底
(1)空气的成分主要以氮气和氧气为主,氧气约占五分之一,氮气约占五分之四,分离液化空气可获得氮气和氧气,氮气化学性质不活泼,因此氮气可用作保护气;故答案为:氧气;化学性质不活泼
(2)利用膜分离技术,在一定压力下让空气通过具有富集氧气功能的薄膜,能得到含氧量较高的富氧空气,该过程发生物理变化,因为没有新物质生成;故答案为:物理
(3)
①通过分析题中所指仪器的作用可知,a是水槽;
②实验室用过氧化氢溶液制取氧气的反应物是固体和液体,反应条件是常温,所以选用的发生装置是:A,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,反应的方程式是:2H2O2
| ||
③用B装置制备氧气的反应物是固体,反应条件是加热,所以可以选用高锰酸钾,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的方程式是:2KMnO4
| ||
④氧气的密度比空气大,所以收集氧气后,取出的集气瓶应正放在实验台上,氧气有助燃性,所以检验氧气是否收集满的方法是:将带火星的木条放在集气瓶口,木条复燃,证明集满;
⑤甲烷难溶于水,密度小于空气,所以收集干燥的甲烷气体要用向下排空气法,选用的装置是:C.
(4)淡黄色的硫粉在空气中燃烧发出淡蓝色的火焰,而在氧气中燃烧,发出蓝紫色火焰,且生成无色有刺激性气味的气体,化学方程式为:S+O2
| ||
(5)铁丝在氧气中剧烈燃烧、火星四射、生成一种黑色固体;在集气瓶底部放少量的水,其目的是防止溅落的熔化物炸裂瓶底,故填:火星四射;防止溅落的熔化物炸裂瓶底;
答案:
(1)氧气;化学性质不活泼
(2)物理
(3)
①水槽;
②A 2H2O2
| ||
③2KMnO4
| ||
④正,将带火星的木条放在集气瓶口,木条复燃,证明集满;
⑤C
(4)刺激性 淡蓝色 S+O2
| ||
(5)火星四射 防止溅落的熔化物炸裂瓶底
点评:本考点考查了空气中各种气体的含量和物理变化与化学变化的辨别等,同学们要加强记忆有关的知识点,在理解的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
相关题目
关于O2、CO2、SO2、H2O2四种物质,下列叙述正确的是( )
| A、都有氧分子 |
| B、一个分子中都含有两个氧原子 |
| C、都是氧化物 |
| D、都是化合物 |
如图表示治理汽车尾气所涉及反应的微观过程.下列说法正确的是( )
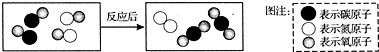

| A、图中单质的化学式为N2 |
| B、该反应使有害气体转化为无害气体 |
| C、该反应属于化合反应 |
| D、该反应分子个数发生了改变,不符合质量守恒定律 |
如图为“XX泉水”商标的一部分,下列说法正确的是( )


| A、该泉水中不含任何化学物质 |
| B、其中钙、镁、钾等是指这些元素的单质 |
| C、该矿泉水中各成分的含量指的是体积分数 |
| D、该矿泉水为混合物 |
 代表硫原子)
代表硫原子)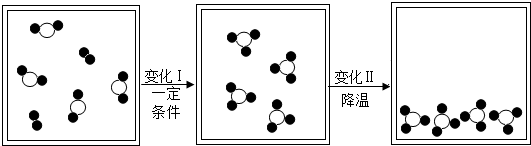
 某同学将浑浊的河水样品倒入烧杯中先加入明矾粉末搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问:
某同学将浑浊的河水样品倒入烧杯中先加入明矾粉末搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问: