题目内容
18.有Fe2O3、CuO、ZnO组成的混和物与足量的CO高温反应,将反应产生的气体通入足量的澄清石灰水中,得沉淀质量为50.0g,金属混合物的质量为24.1g,原固体混合物的质量为( )| A. | 32.1g | B. | 35.9 g | C. | 40.1g | D. | 74.1g |
分析 根据反应方程式判断CO2中的O原子来源于CO和金属氧化物,计算出氧化物中氧元素的质量,金属氧化物的质量等于金属的质量加氧化物中氧元素的质量.
解答 解:设生成的二氧化碳的质量为x.
CO2+Ca(OH)2═CaCO3↓+H20
44 100
x 50.0g
则$\frac{44}{100}=\frac{x}{50.0g}$,解得x=22g
发生的有关反应为:Fe2O3+3CO $\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2,ZnO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Zn+CO2,CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,
二氧化碳中碳元素的质量等于一氧化碳中碳元素的质量,故一氧化碳中碳元素质量为:22g×$\frac{12}{44}×100%$=6g,一氧化碳中氧元素质量为6g×$\frac{16}{12}$=8g,
二氧化碳中氧元素的质量为22g-6g=16g,从反应方程式可以看出,CO2中的O原子来源于CO和金属氧化物,故金属氧化物中氧元素的质量为16g-8g=8g.
所以金属氧化物的质量为24.1g+8g=32.1g.
故选A.
点评 本题考查混合物的质量计算,题目难度较大,注意从元素质量守恒的角度分析.

练习册系列答案
相关题目
8.初中化学中几种常见物质之间的相互转化关系如图所示.已知常温下B、C、E为气体,且B是植物进行光合作用的一种重要原料,E有毒;D、F均为无色液体,都由两种相同的元素组成,且分子中原子个数比依次为2:1和1:1;(部分反应物和生成物及反应条件已略去).下列有关判断不正确的是( )

| A. | E转变为B可以通过与O2发生反应实现 | |
| B. | D、F中氧元素的化合价一定不相同 | |
| C. | A可能是CaCO3 | |
| D. | 除去B中混有的少量的E,可以将混合气体点燃 |
9.某些花岗岩石材中含有放射性氡.氡原子的质子数为86,中子数为136.下列关于氡元素的各种说法中不正确的是( )
| A. | 氡原子的电子数为86 | B. | 氡原子的核电荷数为86 | ||
| C. | 氡原子的相对原子量质量为222g | D. | 氡元素为非金属元素 |
6.下列关于金属的说法正确的是( )
| A. | 人类使用金属铝的年代早于铜、铁 | |
| B. | 生铁和钢是铁的合金,它们之间的差别是含碳量不同,钢的含碳量高 | |
| C. | 武德合金的熔点低,不可用于制造保险丝 | |
| D. | 比较黄铜片与铜片的硬度大小,通常是将两种金属片相互刻画 |
7.类推是化学学习中常用的思维方法.下列类推结果正确的是( )
| A. | 离子是带电的原子或原子团,所以带电的微粒一定是离子 | |
| B. | 同种元素可以组成纯净物,故混合物一定是由不同种元素组成的 | |
| C. | 自燃是由缓慢氧化引起的,则缓慢氧化一定引起自燃 | |
| D. | 硬水中含较多可溶性钙镁化合物,故蒸馏水是软水 |
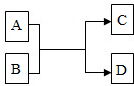 A、B、C、D都是初中化学中常见物质,它们间关系如图所示(反应条件已省略).
A、B、C、D都是初中化学中常见物质,它们间关系如图所示(反应条件已省略).
