题目内容
3.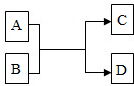 A、B、C、D都是初中化学中常见物质,它们间关系如图所示(反应条件已省略).
A、B、C、D都是初中化学中常见物质,它们间关系如图所示(反应条件已省略).(1)该反应不可能属于分解反应和化合反应;
(2)若A为金属,C为密度最小的气体,则B可能为HCl或H2SO4(填化学式,下同);
(3)若A为CO,C为金属,则D为CO2;
(4)若A为蓝色溶液,C为浅绿色溶液,则D为Fe.
分析 根据反应物、生成物种类可以排除反应类型;
氢气是密度最小的气体,比较活泼的金属能和稀盐酸或稀硫酸反应生成盐和氢气;
高温条件下,某些金属氧化物能和一氧化碳反应生成金属和二氧化碳;
氯化铜、硫酸铜、硝酸铜的溶液是蓝色的,能和铁反应生成铜和氯化亚铁、硫酸亚铁和硝酸亚铁,氯化亚铁、硫酸亚铁和硝酸亚铁的溶液是浅绿色的.
解答 解:(1)反应物和生成物都是两种,该反应不可能是分解反应和化合反应.
故填:分解.(2)若A为金属,C为密度最小的气体,则B可能为稀盐酸或稀硫酸,化学式是HCl或H2SO4.故填:HCl或H2SO4.(3)若A为CO,C为金属,则D为二氧化碳,化学式是CO2.
故填:CO2.
(4)若A为蓝色溶液,C为浅绿色溶液,则D为铁,铁的化学式是Fe.
故填:Fe.
点评 本题主要考查物质的性质,只要掌握了物质的化学性质,解答起来比较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.学习了MnO2对过氧化氢有催化作用的知识后.某同学想:氧化铜(CuO)能否起到类似MnO2的催化剂作用呢?于是进行了如下探究.
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5ml5%的过氧化氢溶液于试管中,进行如下实验:
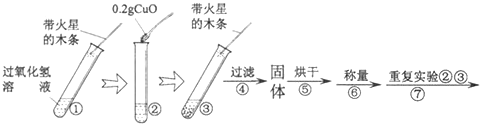
(1)填写下表:
(2)步骤①③(填序号)的目的是证明CuO能加快过氧化氢溶液分解的速率;
(3)步骤⑦的目的是证明CuO的化学性质在反应前后不变;
(4)过氧化氢能被CuO催化分解放出氧气的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气;
(5)请你设计实验比较二氧化锰和CuO的过氧化氢制取氧气实验中的催化效果
实验步骤:常温下,取两份5mL5%的过氧化氢溶液分别加入0.2g的MnO2粉末和CuO粉末(或写颗粒大小相同的MnO2和CuO),(控制2个变量)比较冒泡速率(或相同时间收集氧气体积或收集等体积氧气所需的时间)
实验结论:相同条件下,用MnO2的催化效果比CuO好.
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5ml5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡放出 带火星的木条复燃 | 称量CuO的质量仍为0.2g | 溶液中有大量气泡放出,带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立猜想Ⅲ成立 |
(3)步骤⑦的目的是证明CuO的化学性质在反应前后不变;
(4)过氧化氢能被CuO催化分解放出氧气的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气;
(5)请你设计实验比较二氧化锰和CuO的过氧化氢制取氧气实验中的催化效果
实验步骤:常温下,取两份5mL5%的过氧化氢溶液分别加入0.2g的MnO2粉末和CuO粉末(或写颗粒大小相同的MnO2和CuO),(控制2个变量)比较冒泡速率(或相同时间收集氧气体积或收集等体积氧气所需的时间)
实验结论:相同条件下,用MnO2的催化效果比CuO好.
11.下列鉴别物质的方法,错误的是( )
| A. | 氮气和二氧化碳--燃着的木条 | B. | 铁粉和炭粉--磁铁吸引 | ||
| C. | 食盐水和蒸馏水--加热蒸发 | D. | 铜片和铝片--观察颜色 |
18.有Fe2O3、CuO、ZnO组成的混和物与足量的CO高温反应,将反应产生的气体通入足量的澄清石灰水中,得沉淀质量为50.0g,金属混合物的质量为24.1g,原固体混合物的质量为( )
| A. | 32.1g | B. | 35.9 g | C. | 40.1g | D. | 74.1g |
12.从化学的角度分析,下列做法合理的是( )
| A. | 稀有气体的化学性质不活泼,可作保护气 | |
| B. | 活性炭具有吸附性,净水器中加入活性炭可用来降低水的硬度 | |
| C. | 厨房煤气管道漏气时,立即打开排气扇通风 | |
| D. | 为增加粮食产量,大量使用农药与化肥 |
13.如图所示是某反应前后的微观示意图,“○”和“●”表示两种不同的原子.则该反应( )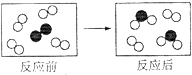

| A. | 是化合反应 | B. | 反应前后分子种类不变 | ||
| C. | 该图示不符合质量守恒定律 | D. | 参加反应的两种分子个数比为4:1 |