题目内容
8.对于反应:X+2NaOH═2Y+Cu(OH)2↓,下列分析中正确的是( )| A. | Y 中钠元素化合价一定为+1价 | B. | X 和Y的相对分子质量之差为18 | ||
| C. | X 可能是CuCl2或CuCO3 | D. | Y 可能是Na2SO4 |
分析 A、根据反应前后钠元素的化合价改变情况进行分析;
B、根据质量守恒定律进行分析;
C、根据在化学反应前后,元素的种类保持不变进行解答;
D、根据复分解反应的原理进行分析.
解答 解:A、依据复分解反应发生的特点,由反应可知当Y是氯化钠时,X应是氯化铜,Y 中钠元素化合价一定为+1价,故A正确;
B、依据质量守恒定律可知,反应前后各物质的相对分子质量之和相等可知,X比2个Y大18,并不能说明X和Y的相对分子质量相差18,故B错误;
C、根据有氢氧化铜生成,所以X中一定含有铜元素,如果X是CuCl2或Cu(NO3)2化学方程式正好相平且符合化学反应的规律,故C错误;
D、根据Y中一定有钠元素,复分解反应是相互交换成分得到的,如果Y是硫酸钠则化学方程式不平,故D错误.
故选:C
点评 在解此类题时,首先分析题中方程式发生的原理,然后结合具体的反应以及物质进行验证即可.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
18.某兴趣小组在学习了双氧水分解制氧气的实验后,知道催化剂(MnO2)能改变化学反应速率.到底还有哪些因素与化学反应速率有关呢?
【小组讨论】甲猜测:化学反应速率与反应物的质量分数有关
乙猜测:化学反应速率与反应温度有关
【设计实验】他们设计并进行了以下4次实验
(1)②和③实验证明甲的观点是正确的,C实验证明乙的观点是正确的(填字母);
A.①和②B.③和④C.①和④
(2)由以上实验还能得出:其他条件相同时,反应温度越高或反应物的质量分数越大,则反应速率越快;
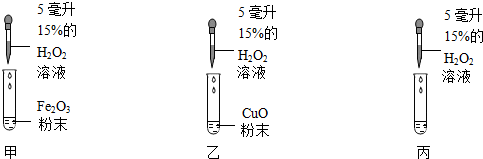
【交流拓展】他们猜测:催化剂 (Mn02)是一种氧化物,那么氧化铁(Fe2O3)、氧化铜(CuO)是否也有这样的催化作用呢?设计了如图的实验.
(3)如果,实验证明氧化铁、氧化铜均有催化作用,那么,小组成员应见到甲、乙均有气泡产生的实验现象.
(4)甲认为,要证明氧化铁、氧化铜是本实验的催化剂,还需要有氧化铁、氧化铜在实验前后质量和化学性质保持不变.
【小组讨论】甲猜测:化学反应速率与反应物的质量分数有关
乙猜测:化学反应速率与反应温度有关
【设计实验】他们设计并进行了以下4次实验
| 实验 次数 | H2O2溶液质 量分数% | H2O2溶液用量 /毫升 | 催化剂(MnO2)用 量/克 | 反应温度 /℃ | 收集气体体积 /毫升 | 所需时间 /秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ④ | 30 | 5 | 0 | 55 | 2 | 10.5 |

(1)②和③实验证明甲的观点是正确的,C实验证明乙的观点是正确的(填字母);
A.①和②B.③和④C.①和④
(2)由以上实验还能得出:其他条件相同时,反应温度越高或反应物的质量分数越大,则反应速率越快;
【交流拓展】他们猜测:催化剂 (Mn02)是一种氧化物,那么氧化铁(Fe2O3)、氧化铜(CuO)是否也有这样的催化作用呢?设计了如图的实验.
(3)如果,实验证明氧化铁、氧化铜均有催化作用,那么,小组成员应见到甲、乙均有气泡产生的实验现象.
(4)甲认为,要证明氧化铁、氧化铜是本实验的催化剂,还需要有氧化铁、氧化铜在实验前后质量和化学性质保持不变.
3.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下反应一段时间后,测得反应前后各物质的质量如下:
试推断容器中的反应式可能是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 20 | 20 | 20 | 20 |
| 反应后质量/g | 20 | 30 | 16 | 14 |
| A. | Z+Q→X+Y | B. | Y→Z+Q | C. | X+Y→Z+Q | D. | Z+Q→Y |
13.将20℃时的硝酸钾饱和溶液密闭加热至50℃,一定发生改变的是( )
| A. | 溶液的质量 | B. | 溶质的质量分数 | C. | 溶质的质量 | D. | 硝酸钾的溶解度 |
20.下列物质敞口存放在桌面上,质量会减小的是( )
| A. | 浓硫酸 | B. | 固体食盐 | C. | 浓盐酸 | D. | 固体氢氧化钠 |
