题目内容
13.根据装置图回答下列问题:
(1)实验室制取较多量的二氧化碳,使用的制气发生装置E(填装置代号),收集装置为B(填装置代号),反应化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,验满的方法是将燃着的木条放于集气瓶口,若木条熄灭,说明收集满了.
(2)实验室用一氧化碳还原氧化铜的化学方程式为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,使用的装置为F(填装置代号),为什么要将尾气烧掉,其原因是一氧化碳有毒,会污染空气.
分析 (1)根据要制取较多量的二氧化碳,则需要较大的反应容器,该反应属于固液常温型,据此 分析解答,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集;检验二氧化碳是否收集满的方法是:将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断.
(2)根据一氧化碳还原氧化铜生成铜和二氧化碳,因为一氧化碳有毒,会污染空气,因此要将尾气烧掉解答.
解答 解:
(1)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,该反应属于固液常温型,且要制取较多量的二氧化碳,需要较大的反应容器,故选发生装置E;二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集;碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;检验二氧化碳是否收集满的方法是:将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;
(2)一氧化碳还原氧化铜生成铜和二氧化碳,化学方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;使用的装置为F;因为一氧化碳有毒,会污染空气,因此要将尾气烧掉;
答案:
(1)E;B;CaCO3+2HCl=CaCl2+H2O+CO2↑;将燃着的木条放于集气瓶口,若木条熄灭,说明收集满了;
(2)CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;F;一氧化碳有毒,会污染空气.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 阅读快车系列答案
阅读快车系列答案| A. | 实验证明水是由氢气和氧气组成的 | |
| B. | 电解水时加入少量硫酸钠或氢氧化钠的目的是增强水的导电性 | |
| C. | 正极和负极产生的气体体积比为2:1 | |
| D. | 负极产生的气体能使带火星的木条复燃 |
| A. | 用硫酸铜可除去铁螺丝表面的铁锈 | B. | 钢铁中只含有金属元素 | ||
| C. | 钢比生铁中碳的含量大 | D. | 废弃的钢铁制品应该回收再利用 |
| A. |  点燃酒精灯 | B. |  检验气密性 | C. |  稀释浓硫酸 | D. |  加热液体 |
| A. |  检查装置的气密性 | B. |  加热液体 | ||
| C. |  气体验满 | D. |  倾倒液体 |
| A. | 给篮球充气,分子之间有间隔 | |
| B. | 夏天湿衣服干的快,温度升高,分子运动加快 | |
| C. | 100ml酒精和100ml水混合后体积小于200ml,分子是有质量的 | |
| D. | 在花园中可闻到花的香味,分子是运动的 |
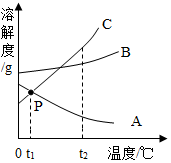 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: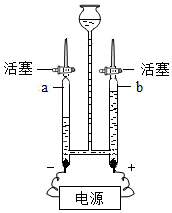 水是人类生活中不可缺少的物质.
水是人类生活中不可缺少的物质.