题目内容
某化合物在氧气中完全燃烧时,消耗了氧气4.8克,同时只生成4.4克的二氧化碳和2.7克水,则该化合物的质量为 克,此化合物所含元素为 (填:元素符号)各元素的质量比为 (与所填元素对应)
| 首先可利用质量守恒定律,计算燃烧过程中化合物的质量;然后根据燃烧的规律,由生成的二氧化碳和水分别计算中化合物中C、H元素质量,由C、H元素质量和与化合物质量对比,判断化合物中是否含有O元素,并由各元素的质量确定化合物中各元素的质量比. | |
| 解答: | 解:根据质量守恒定律,化合物的质量=4.4g+2.7g﹣4.8g=2.3g 4.4g二氧化碳中C元素质量=4.4g× 则2.3g化合物中含C、H元素的质量=1.2g+0.3g=1.5g,因此化合物中除C、H元素外还含有O元素 化合物中C、H、O元素质量比=1.2g:0.3g:(2.3g﹣1.2g﹣0.3g)=12:3:8 故答案为:2.3;CHO;12:3:8. |

练习册系列答案
相关题目
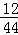 ×100%=1.2g,2.7g水中H元素质量=2.7g×
×100%=1.2g,2.7g水中H元素质量=2.7g×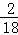 ×100%=0.3g
×100%=0.3g