题目内容
20.实验是学习化学的一个重要途径.如图是实验室常用的实验仪器,请根据它们的用途回答下列有关问题:
(1)写出标号仪器名称:C试管,D酒精灯;
(2)如果用一种纯净物制取并收集氧气,需选择上述仪器中的ACDEFHI(填序号)组装成合适装置,有关反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取二氧化碳可采用的收集方法是向上排空气法.将制得的二氧化碳通入澄清石灰水,观察到的现象是澄清石灰水变浑浊,反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O,该反应可以用来检验二氧化碳.
分析 (1)C、D均为实验室常用的仪器,熟记常用仪器的名称即可解答.
(2)实验室制氧气的三种方法中只有加热高锰酸钾这一方法是用一种纯净物在制取氧气,根据反应物的状态和反应条件确定发生装置,根据气体的密度和溶水性确定收集装置,再根据发生装置和收集装置选择所需要的仪器.
(3)熟记常用的化学方程式;根据气体的密度和溶水性确定气体的收集方法.通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成碳酸钙和水去分析解答;
解答 解:(1)熟记常用仪器的名称可知C为试管;D为酒精灯.
(2)实验室制氧气的三种方法中只有加热高锰酸钾这一方法是用一种纯净物在制取氧气,其反应物的状态是固态,反应条件是加热,应选固-固加热型的方法制取氧气,其发生装置应选用的仪器有ACD,根据试管的开口方向,选用的导气管是F,根据F确定是在用排水法收集,还应选用的仪器有EHI;高锰酸钾加热生成锰酸钾、二氧化锰和氧气.故答案为:ACDEFHI 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳;二氧化碳的密度比空气大,能溶于水,只能用向上排空气法收集.通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成碳酸钙和水,其反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
答案:
(1)C试管;D酒精灯
(2)ACDEFHI 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(3)向上排空气法 澄清石灰水变浑浊 Ca(OH)2+CO2=CaCO3↓+H2O 检验二氧化碳
点评 本道题考查的内容之一是选择合适的仪器组装某个实验需要的装置,要求学生对一些常用实验装置所用的仪器、装置的组装方法、装置的使用方法熟记于心.

 名校课堂系列答案
名校课堂系列答案 下表是元素周期表的一部分:
下表是元素周期表的一部分:| 族 周期 | IA | 0 | ||||||
| 一 | 1 H 1.008 | ⅡA | ⅢA | ⅣA | V A | ⅥA | ⅦA | 2 He 4.003 |
| 二 | 3 Li 6.941 | 4 Be 9.012 | 5 B 10.8l | 6 C 12.01 | 7 N 14.0l | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.18 |
| 三 | 11 Na 22.99 | 12 Mg 24.31 | 13 Al 26.98 | 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 | 18 Ar 39.95 |
(2)X3+的结构示意图如图所示,该元素位于周期表中第三周期,第ⅢA族.
(3)写出原子序数1、6、8、11四种元素组成的化合物的化学式NaHCO3.
| A. | 金属铁中铁元素有0、+2、+3价 | B. | 纯净物都是由同种元素组成的 | ||
| C. | 离子在化学反应中不一定发生变化 | D. | 不同种元素组成的物质才是混合物 |
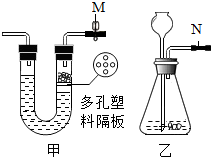
| A. | 此时甲装置中的止水夹M处于关闭状态 | |
| B. | 甲装置具有控制反应的开始与结束的功能 | |
| C. | 乙装置的长颈漏斗下端一定要伸入液体中起液封作用 | |
| D. | 乙装置N处添加止水夹可以与甲装置具有相同功能 |
| A. | 缺碘会引起高血压 | B. | 缺铁会引起贫血 | ||
| C. | 缺钙会引起骨质疏松 | D. | 缺锌会引起发育停滞、智力低下 |
| 选项 | 物质 | 所加试剂(过量) | 操作方法 |
| A | CO2(CO) | O2 | 点燃 |
| B | 铜粉(铁粉) | 稀硫酸 | 过滤 |
| C | CaO(CaCO3) | 盐酸 | 过滤 |
| D | CuSO4溶液(H2SO4) | Cu | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
 蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH2,蚁酸在一定条件下会分解生成两种氧化物
蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH2,蚁酸在一定条件下会分解生成两种氧化物