题目内容
5.已知在某化肥K2SO4样品中可能混入了NH4Cl、NH4NO3、K2CO3三种物质中的一种或多种,为推测混入的物质种类,现按图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全进行).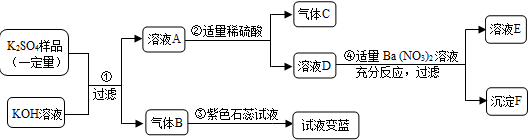
试根据实验过程和发生的现象填写以下空白:
(1)仅根据上述实验现象,NH4Cl、NH4NO3、K2CO3三种物质中,还不能确定是否混入化肥K2SO4样品中物质是NH4Cl、NH4NO3(写化学式)
(2)要进一步推理化肥样品中的物质,可用溶液E再实验,请简要说明实验操作步骤、发生的现象及结论向溶液E中加入硝酸银,如果有白色沉淀生成,说明样品中含有NH4Cl,可能含有NH4NO3;如果没有白色沉淀,则样品中含有NH4NO3,不含有NH4Cl.
分析 根据碳酸根离子与酸能反应生成二氧化碳,所以加入硫酸产生气体,说明含有碳酸根离子;由于碳酸钾与硫酸反应生成硫酸钾和水、二氧化碳;原来也含有硫酸钾,所以硫酸钾再与硝酸钡反应生成硫酸钡沉淀和硝酸钾,所以E中一定含有硝酸钾(KNO3);加入氢氧化钾能产生气体,由于碱性溶液能使紫色石蕊试液变蓝,所以气体B水溶液显碱性,我们学习过去的碱性气体是氨气,与碱溶液产生氨气,说明样品中含有带铵根离子的,只能证明样品中含有带铵根离子的,但不能确定是氯化铵还是硝酸铵;向溶液E中加入硝酸银,如果有白色沉淀生成,说明样品中含有氯离子,据此分析.
解答 解:(1)由于碳酸根离子与酸能反应生成二氧化碳,所以加入硫酸产生气体,说明含有碳酸根离子,所以一定含有碳酸钾(K2CO3);由于碳酸钾与硫酸反应生成硫酸钾和水、二氧化碳;原来也含有硫酸钾,所以硫酸钾再与硝酸钡反应生成硫酸钡沉淀和硝酸钾,所以E中一定含有硝酸钾(KNO3);加入氢氧化钾能产生气体,由于碱性溶液能使紫色石蕊试液变蓝,我们学习过去的碱性气体是氨气,与碱溶液产生氨气,说明样品中含有带铵根离子的,只能证明样品中含有带铵根离子的,但不能确定是氯化铵还是硝酸铵;向溶液E中加入硝酸银,如果有白色沉淀生成,说明样品中含有NH4Cl,因为氯化银属于白色沉淀,所以说明一定含有氯化铵,可能含有NH4NO3;如果没有白色沉淀,则不含有氯离子,则样品中含有NH4NO3,不含有NH4Cl;因此不能确定NH4Cl、NH4NO3;
(2)向溶液E中加入硝酸银,如果有白色沉淀生成,说明样品中含有NH4Cl,因为氯化银属于白色沉淀,所以说明一定含有氯化铵,可能含有NH4NO3;如果没有白色沉淀,则不含有氯离子,则样品中含有NH4NO3,不含有NH4Cl.
故答案为:(1)NH4Cl、NH4NO3;(2)向溶液E中加入硝酸银,如果有白色沉淀生成,说明样品中含有NH4Cl,可能含有NH4NO3;如果没有白色沉淀,则样品中含有NH4NO3,不含有NH4Cl.
点评 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.解答本题关键是要知道碳酸盐与酸反应能生成二氧化碳,铵盐与碱反应能产生氨气.

| A. | 锌置换出氢气有元素化合价变化,则所有置换反应都有元素化合价的变化 | |
| B. | CH4充分燃烧生成的水和二氧化碳,则充分燃烧生成水和二氧化碳的物质一定只含有C、H元素 | |
| C. | 化合反应生成产物只有一种,则生成产物只有一种的一定是化合反应 | |
| D. | 在氯酸钾分解制取氧气中,用二氧化锰做催化剂,则没有催化剂氯酸钾不能生成氧气 |
关注食品安全,购买前请认真阅读食品标签.下表是某品牌钙奶包装袋上的部分内容.
| 品名 | XX牌钙奶饼干 |
| 配料 | 小麦粉、白砂糖、花生油含(维生素E)鲜鸡蛋、奶粉、食品添加剂(碳酸氢铵碳酸氢钠碳酸钙蛋白酶) |
| 保质期 | 8个月 |
| 生产日期 | 2015年10月22 |
①主要提供蛋白质的物质有鲜鸡蛋、奶粉,能提供人体主要供能物质的有小麦粉、白砂糖.
②检验饼干中含有淀粉的方法是取样,滴加碘液,如果变成蓝色,说明饼干中含有淀粉.
(2)配料中的食品添加剂
①碳酸氢钙的作用是使饼干蓬松,烘焙时发生反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
②老年人缺钙会导致骨质疏松症,配料中碳酸钙能提供钙(填“单质”“分子”“元素”)元素.
(3)结合生产日期保质期,最好在保质期内食用完.
 如图所示装置中,U形管中的液面原先左右相平,向试管内的水中加入某种物质后,U形管中的液面变为左高右低,则加入的物质可能是( )
如图所示装置中,U形管中的液面原先左右相平,向试管内的水中加入某种物质后,U形管中的液面变为左高右低,则加入的物质可能是( )| A. | 硝酸铵 | B. | 生石灰 | C. | 氢氧化钠 | D. | 浓硫酸 |
【查阅资料】:碳酸钾与纯碱具有相似的化学性质
【实验探究】:
| 探究过程 | K2CO3) | (NH4)2SO4 | 结论及化学方程式 |
| ①分别取碳酸钾和硫酸铵固体,加入足量水溶解,取溶液分别滴入紫色石蕊溶液,观察溶液颜色变化 | 变蓝 | 变红色 | 碳酸钾溶液显碱性 硫酸铵溶液显酸性 |
| ②另取两种溶液分别加入足量 足量稀盐酸,观察现象 | 产生气泡 | 无明显现象 | 产生气泡的化学方程式 K2CO3+2HCl═2KCl+H2O+CO2↑ |
| ③再取两种溶液分别加入 Ba(OH)2溶液,观察现象 | 产生白色沉淀 | 产生白色沉淀 有刺激性气味的气体生成 | (NH4)2SO4与 Ba(OH)2反应方程式 (NH4)2SO4+Ba(OH)2═BaSO4↓+2H2O+2NH3↑ |
【拓展与延伸】:农民家中的硫酸铵与氯化铵都是白色固体,易混淆,请你设计一方案,帮助农民朋友加以鉴别(操作、现象、结论)分别取少量固体放入试管中加热,固体逐渐变少而消失,原样品为NH4Cl,无明显变化的是Na2SO4.
 小敏同学在实验室中制取CO2气体,为对废液进行后续探究,他向一定质量的含CaCl2和HCl的溶液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液的质量与溶液的pH变化关系如图所示,那么hk段出现的实验现象为产生白色沉淀,在K点的溶液中的溶质为NaCl.
小敏同学在实验室中制取CO2气体,为对废液进行后续探究,他向一定质量的含CaCl2和HCl的溶液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液的质量与溶液的pH变化关系如图所示,那么hk段出现的实验现象为产生白色沉淀,在K点的溶液中的溶质为NaCl.