题目内容
【题目】物质的性质决定物质的用途。氢氧化钙在工农业生产、国防建设等领域用途极广。请回答下列问题:
(1)某化工厂生产过程产生的污水中,主要污染物是盐酸,可用成本较低的熟石灰进行处理。写出该反应的化学方程式:_____。请分析该反应的微观实质:_____。请另外再写出一个符合上述反应实质的化学方程式_____。
(2)在农业上用石灰乳(主要成分是氢氧化钙)和硫酸铜晶体混合配制波尔多液,可防治多种病害。氢氧化钙在农业中还可以用于_____。(请写一种即可)
(3)在国防建设中石灰乳和苦卤水(海水晒盐析出粗盐晶体后剩余的液体)为原料,通过一系列化学变化制得“国防金属”镁。综合利用苦卤水制备金属镁的流程如下图所示,请根据下图回答下列问题:

①要使苦卤水中的MgCl2完全转化为沉淀Mg(OH)2,分批加入过量的石灰乳。使海水中的MgCl2全部转化为Mg(OH)2。写出该反应的化学方程式_____.
②要将沉淀出的氢氧化镁转化为氯化镁,可以加入过量的X溶液,写出X的化学式_____.
③无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式:MgCl2![]() Mg+Cl2↑;反应基本类型是_____。
Mg+Cl2↑;反应基本类型是_____。
【答案】2HCl+Ca(OH)2═CaCl2+2H2O 酸中的氢离子和碱中的氢氧根离子结合生成水分子 HCl+NaOH═NaCl+H2O 改良酸性土壤 Ca(OH)2+MgCl2═Mg(OH)2↓+CaCl2 HCl 分解反应
【解析】
(1)盐酸能与氢氧化钙生成氯化钙和水,该反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成水分子,氢氧化钠与盐酸生成氯化钠和水也是此类反应,故填:2HCl+Ca(OH)2═CaCl2+2H2O;酸中的氢离子和碱中的氢氧根离子结合生成水分子;HCl+NaOH═NaCl+H2O;
(2)氢氧化钙具有碱性,在农业中还可以用于改良酸性土壤,故填:改良酸性土壤;
(3)①要使苦卤水中的MgCl2完全转化为沉淀Mg(OH)2,分批加入过量的石灰乳,使海水中的MgCl2全部转化为Mg(OH)2,使氯化镁与氢氧化钙反应生成氢氧化镁沉淀和氯化钙,故填:Ca(OH)2+MgCl2═Mg(OH)2↓+CaCl2;
②要将沉淀出的氢氧化镁转化为氯化镁,可以加入过量的盐酸,故填:HCl.
③无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为MgCl2![]() Mg+Cl2↑,该反应的特征是一变多,属于分解反应,故填:分解反应.
Mg+Cl2↑,该反应的特征是一变多,属于分解反应,故填:分解反应.

 名校课堂系列答案
名校课堂系列答案【题目】下图中“—”表示相连的物质之间可以在溶液中发生化学反应。下列表中 四组选项中,符合该图要求的是( )
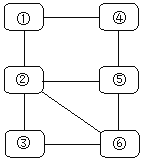
① | ② | ③ | ④ | ⑤ | ⑥ | |
A | 锌 | 稀盐酸 | 碳酸钙 | 硫酸铜 | 烧碱 | 硫酸铁 |
B | 铁 | 稀硫酸 | 氯化钡 | 硝酸铜 | 熟石灰 | 碳酸钠 |
C | 二氧化碳 | 氢氧化钠 | 稀硫酸 | 氢氧化钡 | 氯化铜 | 碳酸钾 |
D | 氧化钙 | 稀盐酸 | 铁 | 稀硫酸 | 碳酸钠 | 氢氧化钡 |
A.AB.BC.C





