题目内容
9.结合图示实验装置,回答下列问题.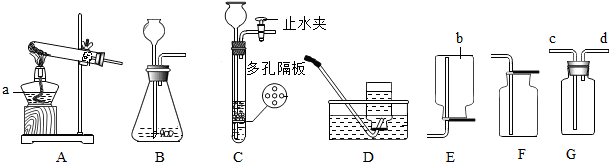
(1)图中a、b仪器的名称:a试管,b集气瓶.
(2)用高锰酸钾固体制氧气,选用的发生装置是A(填“A”、“B”或“C”),反应的化学方程式为
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;如用D装置收集O2,则气体收集完毕时,应先从水中取出导气管(填“从水中取出导气管”或“熄灭酒精灯”);如用F装置收集O2,则验满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(3)实验室制取氢气时,如用G装置收集H2,则气体应从d端通入(填“c”或“d”).
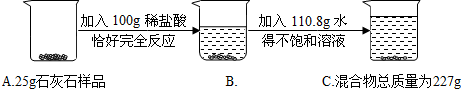
(4)小红同学想探究实验室中用石灰石和稀盐酸反应制取二氧化碳后废液中溶质的成分,请你一同参与探究并回答问题.
【提出问题】废液中的溶质是什么物质?
【作出猜想】小红认为废液中溶质只有CaCl2;你认为还可能含有的溶质是HCl(填化学式).
【查阅资料】CaCl2溶液呈中性.
【实验与结论】①请你写出碳酸钙和盐酸反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
②分别取少量该废液和CaCl2溶液加入到两支试管中,并向其中分别滴入无色酚酞试液做对比实验,结果两支试管中溶液均无色,于是小红认为自己的猜想是正确的.
③你认为小红的实验不能(填“能”或“不能”)证明她的猜想,理由是HCl的存在也不会使酚酞试液变色.
④如果要证明你的猜想是正确的,你可以选择A(填字母)来代替酚酞试液.
A.石蕊试液 B.氢氧化钠溶液 C.稀盐酸 D.硝酸银溶液
 【拓展与应用】①若实验证明了你的猜想是正确的,向废液中加入过量的碳酸钙,反应完成后过滤,即可得到只含CaCl2一种溶质的溶液.
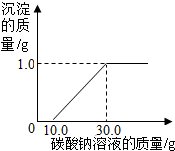
【拓展与应用】①若实验证明了你的猜想是正确的,向废液中加入过量的碳酸钙,反应完成后过滤,即可得到只含CaCl2一种溶质的溶液.②经实验证明了你的猜想是正确.某同学继续做了如下实验:取废液20.0g于烧杯中,逐滴滴入碳酸钠溶液至过量,滴入碳酸钠溶液质量(/g)与生成沉淀的质量 (/g)的变化关系如图所示.试计算:
(ⅰ)废液中CaCl2的质量分数;
(ⅱ)碳酸钠溶液中溶质的质量分数.
分析 试管是常用的反应容器,集气瓶是收集气体的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.小红认为废液中溶质只有CaCl2;我认为还可能是氯化钙和盐酸的混合物;我认为小红的实验不能证明她的猜想,理由是HCl的存在也不会使酚酞试液变色;要证明有盐酸,可以滴加紫色石蕊试液,紫色变红色,就证明有盐酸;若实验证明了我的猜想是正确的,向废液中加入过量的碳酸钙,反应完成后过滤,即可得到只含CaCl2一种溶质的溶液;有关的计算要准确.
解答 解:(1)试管是常用的反应容器,集气瓶是收集气体的仪器,故答案为:试管;集气瓶;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;故答案为:A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;从水中取出导气管;将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
(3)实验室制取氢气时,如用G装置收集H2,则气体应从短管进入,因为氢气的密度比空气小;故答案为:d;
(4)小红认为废液中溶质只有CaCl2;我认为盐酸过量时,还可能是氯化钙和盐酸的混合物;碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,配平即可;我认为小红的实验不能证明她的猜想,理由是HCl的存在也不会使酚酞试液变色;要证明有盐酸,可以滴加紫色石蕊试液,紫色变红色,就证明有盐酸;故答案为:HCl;CaCO3+2HCl=CaCl2+H2O+CO2↑;不能;HCl的存在也不会使酚酞试液变色;A;
【拓展与应用】若实验证明了我的猜想是正确的,向废液中加入过量的碳酸钙,反应完成后过滤,即可得到只含CaCl2一种溶质的溶液;故答案为:①碳酸钙;
②设废液中氯化钙的质量为x,参加反应的碳酸钠的质量为y;
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111 100
y x 1.0g $\frac{111}{100}=\frac{x}{1.0g}$ x=1.11g $\frac{106}{100}=\frac{y}{1.0g}$ y=1.06g;
该废液中CaCl2的质量分数为:$\frac{111g}{20g}×100%$=5.55%
碳酸钠溶液中溶质的质量分数为:$\frac{1.06g}{30g-10g}$×100%=5.3%
答:(ⅰ)该废液中CaCl2的质量分数为5.55%
(ⅱ)碳酸钠溶液中溶质的质量分数为5.3%
故答案为:5.55%;5.3%;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关化学方程式的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 机动车加尾气净化器 | B. | 减少使用化石燃料 | ||
| C. | 农业秸秆集中田间焚烧 | D. | 发展天然气公交线路 |
| A. | 玻璃 | B. | 钢筋混凝土 | C. | 陶瓷 | D. | 聚乙烯塑料 |
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是碳,白色物质可能是Na2O或碳酸钠;
乙同学还认为白色物质是氢氧化钠.甲同学立刻认为乙同学的猜想是错误的,其理由是根据质量守恒定律,反应前没有氢元素.
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O═2NaOH
【实验探究】甲同学对白色物质进行实验探究.
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质是Na2CO3 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
(2)方案2中加入过量的CaCl2溶液的目的是完全除去氯化钙.
【得出结论】钠在二氧化碳中燃烧的化学方程式为4Na+4CO2$\frac{\underline{\;点燃\;}}{\;}$C+2Na2CO3.
通过以上探究,你还能从燃烧的知识获得哪些新认识:燃烧不一定需要氧气.
| A. | 薄荷脑是3种元素组成的有机物 | |
| B. | 1个薄荷脑分子中含有31个原子 | |
| C. | 薄荷脑中碳元素的质量分数大于氢元素的质量分数 | |
| D. | 薄荷脑中碳、氢元素的质量比为1:2 |
【提出问题】促进过氧化氢分解的微粒是什么?
【查阅资料】
1.过氧碳酸钠(Na2CO4)与水反应生成碳酸盐和过氧化氢;
2.可溶性盐在水溶液中都是以金属离子(或NH4+)和酸根离子的形式存在;
【作出猜想】猜想一:促进过氧化氢分解的微粒可能是水分子
猜想二:促进过氧化氢分解的微粒可能是Na+
猜想三:促进过氧化氢分解的微粒可能是CO32-
小松同学指出,不可能是水分子促进了过氧化氢的分解.你赞成(填“赞成”或“不赞成”),你的理由是过氧化氢溶液中就存在水分子,没有加快反应速率.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 | |
| 实验一 | 向6%3mL的过氧化氢溶液中加入1mL 10%的NaCl溶液,深入一根带火星的木条 | 促进过氧化氢分解的微粒不是Na+ | 猜想二不成立 |
| 实验二 | 向 6%3mL的过氧化氢溶液中,加入1mL10%的K2CO3溶液,伸入一根带火星的木条 | 促进过氧化氢分解的微粒是CO32- | 猜想三成立 |