题目内容
1.小明同学对超市一种新产品-“污渍爆炸盐”产生浓厚兴趣,该产品的主要成分是过氧碳酸钠(Na2CO4)在实验室,小明将污渍爆炸盐放入热水中,发现立即产生大量气泡,能使带火星的木条复燃.小明进一步将等浓度的过氧化氢溶液放入相同温度的热水中,发现此时的过氧化氢分解速率明显小于污渍爆炸盐的分解速率.【提出问题】促进过氧化氢分解的微粒是什么?
【查阅资料】
1.过氧碳酸钠(Na2CO4)与水反应生成碳酸盐和过氧化氢;
2.可溶性盐在水溶液中都是以金属离子(或NH4+)和酸根离子的形式存在;
【作出猜想】猜想一:促进过氧化氢分解的微粒可能是水分子
猜想二:促进过氧化氢分解的微粒可能是Na+
猜想三:促进过氧化氢分解的微粒可能是CO32-
小松同学指出,不可能是水分子促进了过氧化氢的分解.你赞成(填“赞成”或“不赞成”),你的理由是过氧化氢溶液中就存在水分子,没有加快反应速率.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 | |
| 实验一 | 向6%3mL的过氧化氢溶液中加入1mL 10%的NaCl溶液,深入一根带火星的木条 | 促进过氧化氢分解的微粒不是Na+ | 猜想二不成立 |
| 实验二 | 向 6%3mL的过氧化氢溶液中,加入1mL10%的K2CO3溶液,伸入一根带火星的木条 | 促进过氧化氢分解的微粒是CO32- | 猜想三成立 |
分析 【作出猜想】过氧碳酸钠(Na2CO4)与水反应生成碳酸钠和过氧化氢;碳酸钠溶于水电离为Na+和CO32-
【设计实验】作对照实验时注意控制变量;
【交流讨论】根据催化剂的特点分析.
解答 解:【作出猜想】碳酸钠溶于水电离为Na+和CO32-;碳酸钠水溶液中含有Na+和CO32-及水分子,所以促进过氧化氢分解的微粒还可能是CO32-;但是水分子不可能促进了过氧化氢的分解,因为过氧化氢溶液中有水分子;
【设计实验】向6%3mL的过氧化氢溶液中加入1mL10%的NaCl溶液,深入一根带火星的木条,若果带火星的木条不复燃,说明促进过氧化氢分解的微粒不是Na+;向6%3mL的过氧化氢溶液中中,加入1mL10%的K2CO3溶液,伸入一根带火星的木条,若果带火星的木条复燃,说明促进过氧化氢分解的微粒是CO32-;
【交流讨论】不正确,没有验证反应前后碳酸钠的化学性质和质量是否发生改变.
故答案为:【作出猜想】CO32-;赞成;过氧化氢溶液中就存在水分子,没有加快反应速率.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 | |
| 实验一 | 向6%3mL的过氧化氢溶液中加入1mL 10%的NaCl溶液,深入一根带火星的木条 | 促进过氧化氢分解的微粒不是Na+ | 猜想二不成立 |
| 实验二 | 向 6%3mL的过氧化氢溶液中,加入1mL10%的K2CO3溶液,伸入一根带火星的木条 | 促进过氧化氢分解的微粒是CO32- | 猜想三成立 |
点评 本题考查的是课本催化剂的知识的拓展探究,完成此题,可以依据已有的知识结合题干提供的信息进行.

练习册系列答案
相关题目
11.一定条件下,在一密闭容器中发生某反应,测得反应过程中各物质的质量如下表所示:
下列判断正确的是( )
| 物 质 | X | Y | Q | Z |
| 第一次测得的质量/g | 32 | 51 | 漏测 | 6 |
| 第二次测得的质量/g | 60 | 17 | 11 | 12 |
| A. | 该反应中X和Q的质量比为5:1 | B. | 该反应可表达为:Y→X+Z+Q | ||
| C. | Q可能是该反应的催化剂 | D. | 该反应可能是置换反应 |
12.不法商家为了让海带碧绿,用化工色素“碱性品绿”进行泡制,还加入了“连二亚硫酸钠Na2S2O4”起固色作用,若长期食用会对肝脏造成损害.Na2S2O4中硫元素的化合价是( )
| A. | +3 | B. | -2 | C. | +4 | D. | +6 |
16.地球大气的演化经历了原始大气、次生大气和现在大气三个阶段,次生大气中部分成分的微观示意图如图:
一定条件下,3.4g甲物质和4.8g氧气恰好完全反应,生成5.4g乙物质和另一种物质X,下列判断不正确的是( )
| 甲 | 乙 | 丙 |  |
 |  |  |
| A. | 物质甲的化学式是NH3 | |
| B. | 物质X的质量为2.8g | |
| C. | 物质X含两种元素 | |
| D. | 该反应化学方程式中物质X与O2的化学计量之比为3:2 |
6.化学用语书写正确的是( )
| A. | 硝酸镁-MgNO3 | B. | 1个二氧化硫分子-SO2 | ||
| C. | 3个氧原子-O3 | D. | 铵根-NH3 |
13.下列各组物质在溶液中能大量共存且能得到无色溶液的是( )
| A. | Na2SO4、NaCl、BaCl2 | B. | H2SO4、NaCl、KNO3 | ||
| C. | CuSO4、KCl、HCl | D. | HCl、NaOH、NaCl |
10.下列实验所对应的方案正确的是( )
| 选项 | 目的 | 方案 |
| A | 除去木炭粉中的氧化铜 | 在空气中充分燃烧 |
| B | 分离NaCl和CaCO3的混合物 | 加足量稀盐酸,蒸发 |
| C | 区分稀盐酸和稀氢氧化钠溶液 | 分别测溶液的pH |
| D | 鉴别化肥NH4Cl和NH4NO3 | 取样,加熟石灰研磨 |
| A. | A | B. | B | C. | C | D. | D |
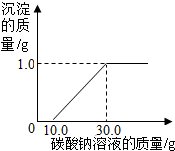 【拓展与应用】①若实验证明了你的猜想是正确的,向废液中加入过量的碳酸钙,反应完成后过滤,即可得到只含CaCl2一种溶质的溶液.
【拓展与应用】①若实验证明了你的猜想是正确的,向废液中加入过量的碳酸钙,反应完成后过滤,即可得到只含CaCl2一种溶质的溶液.