题目内容
 我校化学兴趣小组就空气中氧气的含量进行实验探究:
我校化学兴趣小组就空气中氧气的含量进行实验探究:【集体讨论】:
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体.他们应该选择(填编号)
A.蜡烛 B.红磷 C.硫粉
为了充分消耗容器中的氧气,药品的用量应保证
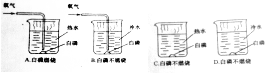
(2)测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号.用弹簧夹夹紧乳胶管.点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧.
①写出红磷在空气中燃烧的化学方程式:
②待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处.由此可知氧气约占空气总体积的
③红磷熄灭后,集气瓶内剩下的气体主要是
考点:测定空气里氧气含量的探究
专题:科学探究
分析:(1)蜡烛燃烧生成水和二氧化碳等物质,红磷燃烧生成五氧化二磷,硫燃烧生成二氧化硫;
(2)磷在空气中燃烧生成五氧化二磷;
根据实验现象可以判断氧气中空气中的含量;
氮气的化学性质比较稳定,不能燃烧,不支持燃烧.
(2)磷在空气中燃烧生成五氧化二磷;
根据实验现象可以判断氧气中空气中的含量;
氮气的化学性质比较稳定,不能燃烧,不支持燃烧.
解答:解:(1)蜡烛、硫粉燃烧都能够生成气体,不能用于测定空气中氧气的含量,而红磷燃烧生成固体五氧化二磷,可以用于测定空气中氧气的含量;为了充分消耗容器中的氧气,药品的用量应保证过量.故填:B;过量.
(2)①该反应的化学方程式为:4P+5O2
2P2O5.故填:4P+5O2
2P2O5.
②打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处.由此可知氧气约占空气总体积的五分之一.故填:五分之一.
③红磷熄灭后,集气瓶内剩下的气体主要是氮气,该气体不支持燃烧.故填:氮气.
故答案为:
(1)B;过量.
(2)①4P+5O2
2P2O5.②五分之一.③氮气.
(2)①该反应的化学方程式为:4P+5O2
| ||
| ||
②打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处.由此可知氧气约占空气总体积的五分之一.故填:五分之一.
③红磷熄灭后,集气瓶内剩下的气体主要是氮气,该气体不支持燃烧.故填:氮气.
故答案为:
(1)B;过量.
(2)①4P+5O2
| ||
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
点燃的火柴竖直向上,火柴杆不易继续燃烧,其原因是( )
| A、火柴杆温度达不到着火点 |
| B、火柴杆着火点高 |
| C、火柴杆潮湿,不易继续燃烧 |
| D、火柴杆接触的氧气少 |
下列物质间的转化关系正确的是( )
①CuO+H2SO4→CuSO4+Na2CO3→CuCO3 ②Fe+O2
Fe2O3+H2SO4→Fe2(S04)3
③CaO+H2O→Ca(OH)2+Na2CO3→CaCO3.
①CuO+H2SO4→CuSO4+Na2CO3→CuCO3 ②Fe+O2
| 点燃 |
③CaO+H2O→Ca(OH)2+Na2CO3→CaCO3.
| A、①② | B、②③ | C、①③ | D、①②③ |
下列二氧化碳的叙述错误的是( )
| A、环境监测中心在公布城市空气质量状况时不包括该气体 |
| B、是造成全球气候变暖的主要气体 |
| C、在蔬菜大棚中,适量补充其含量有利于农作物的生长 |
| D、能与血红蛋白结合,使血红蛋白携氧能力降低 |
下列情况发生了化学变化过程中的吸热反应的是( )
| A、木材起火时用水浇灭 |
| B、图书资料起火时用CO2灭火器喷灭 |
| C、将红热的木炭放入CO2气体中变成了CO |
| D、将镁条放入盐酸中剧烈反应 |