题目内容
已知一个质子的质量为1.6726×10-27kg,一个中子的质量为1.6749×10-27kg,一个电子的质量是一个质子质量的
,一个碳原子质量的
为1.66×10-27kg,请以氧原子为例,用数学计算过程证明:相对原子质量=质子数+中子数.
| 1 |
| 1836 |
| 1 |
| 12 |
考点:相对原子质量的概念及其计算方法
专题:物质的微观构成与物质的宏观组成
分析:相对原子质量是以一个碳-12原子质量的
作为标准,任何一个原子的实际质量跟一个碳-12原子质量
的比值,为该原子的相对原子质量;
| 1 |
| 12 |
| 1 |
| 12 |
解答:解:氧原子的质量为2.657×10-26kg,其相对原子质量为:(2.657×10-26kg)÷(1.66×10-27kg)=16;
而一个质子的相对原子质量为:(1.6726×10-27kg)÷(1.66×10-27kg)=1;一个中子的相对原子质量为:(1.6749×10-27kg)÷(1.66×10-27kg)=1;
而一个氧原子含有8个质子和8个中子,由此知,氧原子的相对原子质量=1×8+1×8=16;
至此,以氧原子为例,用数学计算过程证明了:相对原子质量=质子数+中子数.
而一个质子的相对原子质量为:(1.6726×10-27kg)÷(1.66×10-27kg)=1;一个中子的相对原子质量为:(1.6749×10-27kg)÷(1.66×10-27kg)=1;
而一个氧原子含有8个质子和8个中子,由此知,氧原子的相对原子质量=1×8+1×8=16;
至此,以氧原子为例,用数学计算过程证明了:相对原子质量=质子数+中子数.
点评:解答本题关键是要知道原子核、质子数、中子数、电子数、相对原子质量各量之间的关系.

练习册系列答案
相关题目
某有机物R在足量氧气中完全燃烧后的化学方程式如下:2R+13O2
8CO2+10H2O.根据质量守定律,R的化学式为( )
| ||
| A、C4H10 |
| B、CH4 |
| C、CH4O |
| D、C2H4O2 |
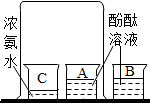 氨分子扩散的实验:
氨分子扩散的实验: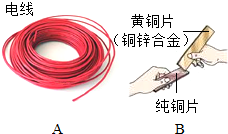 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛.