题目内容
 过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用,某化学研究性学习小组设计并完成了如下实验.
过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用,某化学研究性学习小组设计并完成了如下实验.【实验目的】测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度.
【实验原理】2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O
【实验装置】
【交流与讨论】
①甲同学认为测定产物中O2的体积即可测定样品的纯度.装置②的作用是:
②乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度.但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是;
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
③丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,得到0.1mol氯化钠.则该样品的中过碳酸钠的质量分数为多少?(写出计算过程)
考点:实验探究物质的组成成分以及含量,气体的净化(除杂),盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:①根据实验原理2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O,要测定氧气的量,必须先除去二氧化碳、氯化氢气体等,再根据实验装置图即可得出答案;二氧化碳能使澄清石灰水变浑浊,可利用此现象鉴别二氧化碳;
②理论上可以根据生成二氧化碳的量求样品纯度,但是实际上难以通过实验测得纯净的二氧化碳的质量,因为反应前后装置②的质量差中还包括氯化氢和水蒸气的质量;所以难以求解;
③根据化学方程式中氯化钠与过碳酸钠的质量关系,即可列比例求解样品中的过碳酸钠的质量.
②理论上可以根据生成二氧化碳的量求样品纯度,但是实际上难以通过实验测得纯净的二氧化碳的质量,因为反应前后装置②的质量差中还包括氯化氢和水蒸气的质量;所以难以求解;
③根据化学方程式中氯化钠与过碳酸钠的质量关系,即可列比例求解样品中的过碳酸钠的质量.
解答:解:
①图中装置②中浓氢氧化钠的作用是除去二氧化碳和氯化氢气体;装置③中澄清石灰水的作用是验证二氧化碳是否被除尽;
②测得二氧化碳的体积偏大,原因可能有:浓盐酸易挥发,产生的氯化氢气体被装置②吸收;二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收;装置①、②内空气中的二氧化碳被装置②吸收;故选ABC.
③设样品中过碳酸钠的质量为y,已知“得到0.1mol氯化钠”,则为5.85g.
2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O
244 234
y 5.85g
则
=
,解得y=6.1g
该样品的纯度为:
×100%=48.8%
故答案为:
①除去二氧化碳和氯化氢气体;验证二氧化碳是否被除尽;②ABC;③48.8%
①图中装置②中浓氢氧化钠的作用是除去二氧化碳和氯化氢气体;装置③中澄清石灰水的作用是验证二氧化碳是否被除尽;
②测得二氧化碳的体积偏大,原因可能有:浓盐酸易挥发,产生的氯化氢气体被装置②吸收;二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收;装置①、②内空气中的二氧化碳被装置②吸收;故选ABC.
③设样品中过碳酸钠的质量为y,已知“得到0.1mol氯化钠”,则为5.85g.
2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O
244 234
y 5.85g
则
| 244 |
| y |
| 234 |
| 5.85g |
该样品的纯度为:
| 6.1g |
| 12.5 |
故答案为:
①除去二氧化碳和氯化氢气体;验证二氧化碳是否被除尽;②ABC;③48.8%
点评:本题考查实验装置和混合物中样品纯度的计算.有关化学方程式的计算,要注意带入方程式计算的必须是实际参加反应或实际生成的物质质量,否则就会造成实验结果的偏大或偏小.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的用途由其化学性质决定的是( )
| A、石墨用作润滑剂 |
| B、氧气用于金属切割 |
| C、铜用于制作电线 |
| D、干冰用于人工降雨 |
化学在能源、材料和环境等研究领域发挥着重要作用.下列说法正确的是( )
| A、化石燃料是可再生能源 |
| B、二氧化碳、甲烷和淀粉都属于有机物 |
| C、合金、合成纤维和合成橡胶都是合成材料 |
| D、太阳能、风能和地热能的利用都有利于保护环境 |

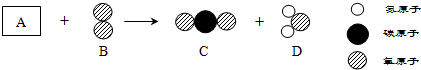
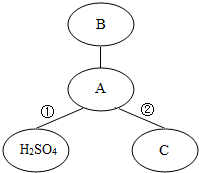 如图中,相连的两种物质间能发生化学反应.请回答有关的问题:
如图中,相连的两种物质间能发生化学反应.请回答有关的问题: 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用. 九月金秋,黑龙江省广袤的黑土地上到处洋溢着丰收的喜悦.今年我省粮食总产将再创历史新高,预计将实现粮食增量、总产量、商品量和调出量四项全国第一.(1)某一块地域的小麦在生长过程中出现叶尖发黄的现象,专家说这是由于小麦生长时缺少一种化肥,这种化肥是①
九月金秋,黑龙江省广袤的黑土地上到处洋溢着丰收的喜悦.今年我省粮食总产将再创历史新高,预计将实现粮食增量、总产量、商品量和调出量四项全国第一.(1)某一块地域的小麦在生长过程中出现叶尖发黄的现象,专家说这是由于小麦生长时缺少一种化肥,这种化肥是①