题目内容
把8克O2和6克C单质放入一密闭的容器中,在一定条件下充分反应,当两种物质都全部消耗时,容器内存在的物质是( )
| A、CO |
| B、C CO2 |
| C、CO O2 |
| D、CO2 O2 |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:依据氧气和碳反应可能会生成二氧化碳和一氧化碳,依据两者的反应方程式中两者的比例即可求出哪一种物质有剩余;
解答:解:碳在氧气充足的时候能够生成二氧化碳,方程式为C+O2
CO2;该反应中碳和氧气的质量比是3:8;碳在氧气不足的时候能够生成一氧化碳,反应方程式为2C+O2
2CO;该反应中碳和氧气的质量比是3:4;把8克O2和6克C单质放入一密闭的容器中,正好是氧气和碳的质量比是4:3,则生成物只有一氧化碳;故容器内的物质是一氧化碳;
故选:A.
| ||
| ||
故选:A.
点评:此题是对化学方程式计算的考查,解题的关键是掌握碳和氧气反应的两种情况中碳和氧气的反应的质量比.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质属于纯净物的是( )
| A、无尘空气 |
| B、加碘食盐 |
| C、高锰酸钾燃烧的剩余物 |
| D、空气中的氧气 |
图中保持水的化学性质的最小微粒是( )
A、 |
B、 |
C、 |
D、 |
下列说法正确的是( )
| A、氧化反应一定是化合反应 |
| B、分子可分、原子不可分 |
| C、含氧元素的化合物是氧化物 |
| D、春天闻到花香,说明分子是不断运动的 |

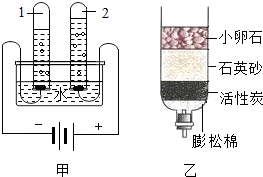 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任. 某校兴趣小组想亲身感受科学家的探究历程,他们选择了《空气中氧气含量的粗略测定》为探究内容.
某校兴趣小组想亲身感受科学家的探究历程,他们选择了《空气中氧气含量的粗略测定》为探究内容.