题目内容
13.实验室常用下列装置研究气体的制取和性质,根据所学知识回答下列问题.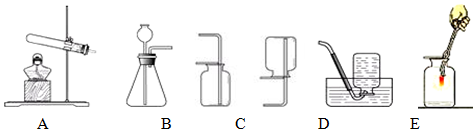
(1)写出实验室制取氧气的一个化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
利用该反应制取氧气,发生装置应选B(填序号,下同).
(2)一氧化氮气体难溶于水,在空气中容易发生下列反应2NO+O2═2NO2,则收集一氧化氮气体时不能用的装置是(填序号)C.
(3)按图F作细铁丝在氧气中燃烧的实验,我观察到的现象有剧烈燃烧或火星四射或放出热量或生成黑色固体(只答一条),化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
实验室里将制得的二氧化碳气体通入澄清石灰水中,始终未出现浑始浊现象,可能的原因是:猜想1装置不严密,二氧化碳气体逸出
猜想2二氧化碳气体中混有氯化氢气体
你能设计实验证明你的猜想吗?每证明一个猜想加2分(附加题)
| 实验步骤 | 实验现象 | 实验结论 |
| 将生成的气体先通过饱和碳酸氢钠溶液,再通过澄清的石灰水 | 澄清石灰水变浑浊 | 二氧化碳气体中混有氯化氢气 |
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.一氧化氮气体难溶于水,在空气中容易发生下列反应2NO+O2═2NO2,则收集一氧化氮气体时不能用排空气法;细铁丝在氧气中燃烧的实验现象是:剧烈燃烧、火星四射、放出热量、生成黑色固体;铁和氧气在点燃的条件下生成四氧化三铁,配平即可.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室里将制得的二氧化碳气体通入澄清石灰水中,始终未出现浑始浊现象,可能的原因是:猜想1装置不严密,二氧化碳气体逸出;猜想2二氧化碳气体中混有氯化氢气体;验证猜想2:将生成的气体先通过饱和碳酸氢钠溶液,再通过澄清的石灰水;澄清石灰水变浑浊;证明二氧化碳气体中混有氯化氢气体.
解答 解:(1)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;B;(合理即可)
(2)一氧化氮气体难溶于水,在空气中容易发生下列反应2NO+O2═2NO2,则收集一氧化氮气体时不能用排空气法;故答案为:C;
(3)细铁丝在氧气中燃烧的实验现象是:剧烈燃烧、火星四射、放出热量、生成黑色固体;铁和氧气在点燃的条件下生成四氧化三铁,配平即可;实验室里将制得的二氧化碳气体通入澄清石灰水中,始终未出现浑始浊现象,可能的原因是:猜想1装置不严密,二氧化碳气体逸出;猜想2二氧化碳气体中混有氯化氢气体;验证猜想2:将生成的气体先通过饱和碳酸氢钠溶液,再通过澄清的石灰水;澄清石灰水变浑浊;证明二氧化碳气体中混有氯化氢气体;故答案为:剧烈燃烧或火星四射或放出热量或生成黑色固体;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;装置不严密,二氧化碳气体逸出;二氧化碳气体中混有氯化氢气体;将生成的气体先通过饱和碳酸氢钠溶液,再通过澄清的石灰水;澄清石灰水变浑浊;二氧化碳气体中混有氯化氢气体;
点评 本考点主要考查了铁在氧气中燃烧的现象、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、有关的实验探究等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
| A. | 在20℃时,x、y的溶液中溶质的质量分数相同 | |
| B. | 温度大于30℃时,x的溶解度大于y的溶解度 | |
| C. | 当x中含有少量y时,可用降低x饱和溶液温度的方法提纯x | |
| D. | 同质量的x、y饱和溶液从30℃降到10℃时,析出的y少于x |
| A. | .酥脆的饼干放置在空气中变软 | B. | 夏天从冰箱取出的冰糕冒“白气” | ||
| C. | 冬季的早晨看到玻璃上有“冰花” | D. | 进入久未开启的菜窖使人感到头昏 |

| A. | 都是化合反应 | B. | 都是氧化反应 | C. | 都需要点燃 | D. | 生成物都是固体 |
A.绿色 B.黑色 C.紫黑色 D.白色
| 物质 | 氧化铜 | 氧化镁 | 碱式碳酸铜 | 碳酸氢铵 |
| 颜色 |

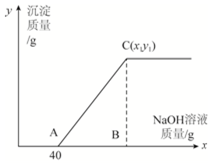 有盐酸和氯化铜的混合溶液共100g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液,生成的沉淀与加入的10%的氢氧化钠溶液的质量关系如图所示.若氯化铜在原混合溶液中的质量分数为13.5%.求:
有盐酸和氯化铜的混合溶液共100g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液,生成的沉淀与加入的10%的氢氧化钠溶液的质量关系如图所示.若氯化铜在原混合溶液中的质量分数为13.5%.求: