题目内容
11.汽车是现代生活中不可缺少的代步工具.请回答下列问题??(1)汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和导电性.?
(2)铁在潮湿的空气中容易锈蚀.
①汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝氧气和水.
②喷漆前需将铁制品放入稀盐酸中除锈,铁锈主要成分是Fe2O3,观察到溶液变黄,有无色气泡逸出,溶液变黄反应的化学方程式是Fe2O3+6HCl═2FeCl3+3H2O.?
分析 根据已有的知识进行分析解答,物质的性质决定物质的用途,铁在与水和氧气并存时易生锈,防锈就是破坏铁生锈的条件,氧化铁能与盐酸反应生成氯化铁和水,据此解答.
解答 解:(1)汽车电路中的导线是利用了金属铜的延展性和导电性,故填:导电.?
(2)①汽车表面喷漆的防锈原理是隔绝氧气和水,故填:氧气.
②氧化铁能与盐酸反应生成氯化铁和水,氯化铁的水溶液呈黄色,故填:Fe2O3+6HCl═2FeCl3+3H2O.?
点评 本题考查的是金属的应用的知识,完成此题,可以依据已有的金属的性质进行.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
1.甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取10g样品溶于一定量的水中得到50g溶液,再分别加入质量不同,溶质质量分数均为10%的氢氧化钠溶液,反应得到沉淀的实验数据如表:
试回答下列问题:
(1)上述实验中,丙同学所用的氢氧化钠溶液一定过量.
(2)求样品中氯化镁的质量(写出计算过程).$\frac{10g-9.5g+11.7g}{50g+80g-5.8g}$
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数.(结果精确到0.01%)
| 甲 | 乙 | 丙 | |
| 加入氢氧化钠溶液质量 (g) | 70 | 80 | 90 |
| 反应得到沉淀的质量 (g) | 5 | 5.8 | 5.8 |
(1)上述实验中,丙同学所用的氢氧化钠溶液一定过量.
(2)求样品中氯化镁的质量(写出计算过程).$\frac{10g-9.5g+11.7g}{50g+80g-5.8g}$
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数.(结果精确到0.01%)
6.除去下列各物质中少量杂质的方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | 稀HCl | H2S04 | 适量BaCl2溶液、过滤 |
| B | KOH溶液 | KCl | 适量HCl |
| C | NaCl溶液 | Na2C03 | 适量Ca(N03)2溶液、过滤 |
| D | C02 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
16.下列判断正确的是( )
| A. | 使酚酞试液变红的溶液是碱性溶液 | |
| B. | PH越小,酸性越弱 | |
| C. | 证明溶液里面含有Cl-,只需要加入AgNO3溶液 | |
| D. | PH<7的雨水叫酸雨 |
3.物质的用途与性质密切相关,下列说法不正确的是( )
| A. | C、CO、H2常用来冶炼金属,是因为它们都具有还原性 | |
| B. | 洗涤剂常用来洗涤油污,是因为洗涤剂有乳化功能 | |
| C. | 铁制栏杆表面常涂“银粉漆”(铝粉)防生锈,是由于铝的化学性质比铁稳定 | |
| D. | 氮气常用作保护气,是由于氮气的化学性质不活泼 |
20.点燃的火柴棍燃烧端朝上时,其未燃尽便熄灭的主要原因是( )
| A. | 缺乏氧气 | |
| B. | 火柴棍的着火点升高了 | |
| C. | 缺乏可燃物 | |
| D. | 燃烧端下方的火柴棍温度不易达到着火点 |
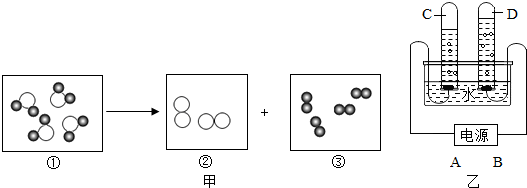
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子.
”表示氧原子.