题目内容
某同学设计了如图所示气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色.请看图回答问题

(1)A中反应的化学方程式 ,B中白磷不燃烧,原因是 .
(2)C中看到的现象是 ;D中看到的现象是 ,D中发生反应的化学方程式为 .
(3)用化学方程式表示E中颜色变化的原因 ,用F装置收集气体的依据是 .
(4)F装置中收集的气体在实验室中是否也能用排水法收集 (填“是”或“否”).

(1)A中反应的化学方程式
(2)C中看到的现象是
(3)用化学方程式表示E中颜色变化的原因
(4)F装置中收集的气体在实验室中是否也能用排水法收集
考点:实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式,燃烧与燃烧的条件
专题:综合实验题
分析:(1)由题意知,反应物双氧水,生成物水和氧气,反应条件为二氧化锰做催化剂,故可书写其化学方程式;根据燃烧的条件分析B中白磷不能够燃烧的原因;
(2)氧气流进入C,气压增大,则把盐酸压入D和石灰石反应生成二氧化碳,据反应原理分析解答;
(3)二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;用F装置是向上排空气法,适合收集密度比空气大的气体;
(4)二氧化碳能溶于水,不能用排水法收集.
(2)氧气流进入C,气压增大,则把盐酸压入D和石灰石反应生成二氧化碳,据反应原理分析解答;
(3)二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;用F装置是向上排空气法,适合收集密度比空气大的气体;
(4)二氧化碳能溶于水,不能用排水法收集.
解答:解:(1)由题意知,反应物双氧水,生成物水和氧气,反应条件为二氧化锰,故反应的方程式为:2H2O2
2H2O+O2↑;B中白磷没能够燃烧的原因是白磷虽然与氧气接触,但温度没有达到白磷的着火点;
(2)氧气流进入C,装置内的气压增大,则把盐酸压入D中和石灰石反应生成二氧化碳,因此观察到的现象是:C中液面下降;D中有液体进入且产生气泡;稀盐酸和石灰石反应生成氯化钙、水和二氧化碳,反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;反应的化学方程式为:CO2+H2O=H2CO3;F装置收集气体是向上排空气法,适合收集密度比空气大的气体,故收集气体的依据是气体密度比空气密度大.
(4)二氧化碳能溶于水,不能用排水法收集;
故答案为:
(1)2H2O2
2H2O+O2↑;温度没有达到白磷的着火点;
(2)C中液面下降;D中有液体进入且产生气泡;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)CO2+H2O=H2CO3;气体密度比空气密度大;
(4)否.
| ||
(2)氧气流进入C,装置内的气压增大,则把盐酸压入D中和石灰石反应生成二氧化碳,因此观察到的现象是:C中液面下降;D中有液体进入且产生气泡;稀盐酸和石灰石反应生成氯化钙、水和二氧化碳,反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;反应的化学方程式为:CO2+H2O=H2CO3;F装置收集气体是向上排空气法,适合收集密度比空气大的气体,故收集气体的依据是气体密度比空气密度大.
(4)二氧化碳能溶于水,不能用排水法收集;
故答案为:
(1)2H2O2
| ||
(2)C中液面下降;D中有液体进入且产生气泡;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)CO2+H2O=H2CO3;气体密度比空气密度大;
(4)否.
点评:本题是综合性较强,考查了气体制取、收集、性质、反应原理等,解决本题需要掌握氧气的反应原理、二氧化碳的实验室制法及其物理性质和化学性质、及可燃物燃烧的条件等知识.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
含铁的混合物5.6g,与足量的盐酸完全反应时放出氢气0.21g.则铁中混入的另一种金属可能是( )
| A、铝 | B、铜 | C、锌 | D、银 |
某气体完全燃烧,产物中含有二氧化碳和水,则该气体组成中( )
| A、可能含有碳、氧元素 |
| B、一定含有氧元素 |
| C、一定含有碳、氢二种元素 |
| D、可能含有碳、氢、氧元素 |
明矾净化水的作用是( )
| A、使硬水软化 |
| B、除去水中的异味 |
| C、除去水中的悬浮物 |
| D、消毒杀菌和净化水 |
利用铝合金代替铝制钥匙是利用铝合金比铝的( )
| A、熔点低 | B、不易腐蚀 |
| C、硬度大 | D、密度小 |
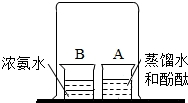 如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞溶液,在小烧杯B中装入30mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起.过一段时间烧杯A中溶液变红色,该实验说明分子具有的性质是
如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞溶液,在小烧杯B中装入30mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起.过一段时间烧杯A中溶液变红色,该实验说明分子具有的性质是