题目内容
 有一黑紫色的固体为KMnO4和MnO2的混合物,为测定混合物中KMnO4的质量分数,某同学取样35.0g,对固体充分加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
有一黑紫色的固体为KMnO4和MnO2的混合物,为测定混合物中KMnO4的质量分数,某同学取样35.0g,对固体充分加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
| 反应时间/min | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
| 剩余固体质量/g | 34.2 | 33.4 | 32.6 | 31.8 | 31.8 |
(1)请问反应到______min时反应完毕.
(2)完全反应后,生成氧气的质量为______g;
(3)求该样品中KMnO4的质量.(精确到小数点后一位).
(4)请在表中画出生成氧气的变化趋势图.
解:(1)依据加热达到4min时5min时固体质量不再减小,所以4.0min时已经反应完毕;
(2)生成的氧气的质量=35.0g-31.8g=3.2g;
(3)设:样品中KMnO4的质量为x
2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
316 32
x 3.2g
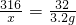
x=31.6g
(4)依据质量守恒定律可得不同时间的氧气量的对应关系:
所以绘制图象如图: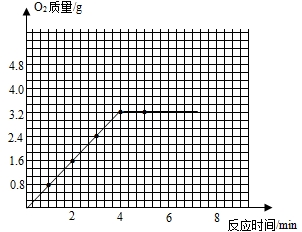 ;
;
故答案为:(1)4;(2)3.2;(3)该样品中KMnO4的质量为31.6g;(4)如图:
分析:(1)依据加热达到4min时固体质量不再减小,所以此时反应完毕;
(2)由于该反应中只有氧气是气体能够使反应后固体质量减小,所以依据质量守恒定律解决即可;
(3)根据氧气的质量即可利用方程式计算出高锰酸钾的质量;
(4)依据1.0min-4.0min的生成的氧气的质量绘制图象即可;
点评:本题主要考查了根据化学方程式的计算和质量守恒定律的应用;本题难度不大,但很容易出错,在分析题目时一定注意量的关系.
(2)生成的氧气的质量=35.0g-31.8g=3.2g;
(3)设:样品中KMnO4的质量为x
2KMnO4
 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑316 32
x 3.2g
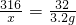
x=31.6g
(4)依据质量守恒定律可得不同时间的氧气量的对应关系:
| 反应时间/min | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
| 剩余固体质量/g | 0.8 | 1.6 | 2.4 | 3.2 | 3.2 |
 ;
;故答案为:(1)4;(2)3.2;(3)该样品中KMnO4的质量为31.6g;(4)如图:

分析:(1)依据加热达到4min时固体质量不再减小,所以此时反应完毕;
(2)由于该反应中只有氧气是气体能够使反应后固体质量减小,所以依据质量守恒定律解决即可;
(3)根据氧气的质量即可利用方程式计算出高锰酸钾的质量;
(4)依据1.0min-4.0min的生成的氧气的质量绘制图象即可;
点评:本题主要考查了根据化学方程式的计算和质量守恒定律的应用;本题难度不大,但很容易出错,在分析题目时一定注意量的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
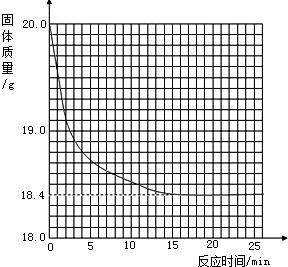 有一黑紫色的固体为KMnO4和MnO2的混合物,为测定混合物中KMnO4的质量分数,某同学取样20.0g,对固体充分加热,测得固体质量随反应时间变化的曲线见下图.
有一黑紫色的固体为KMnO4和MnO2的混合物,为测定混合物中KMnO4的质量分数,某同学取样20.0g,对固体充分加热,测得固体质量随反应时间变化的曲线见下图.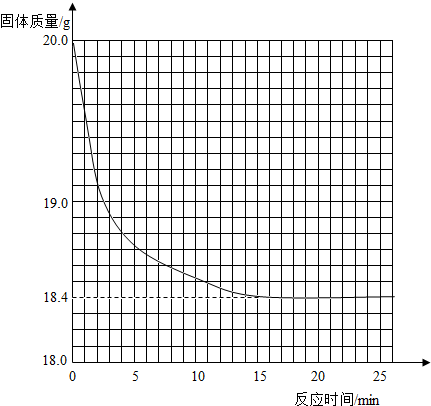
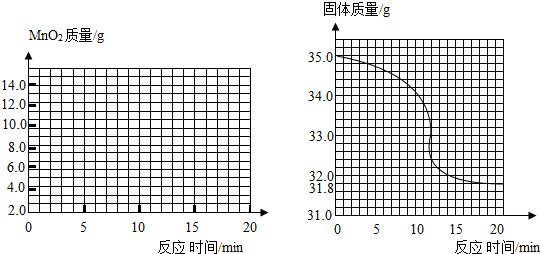

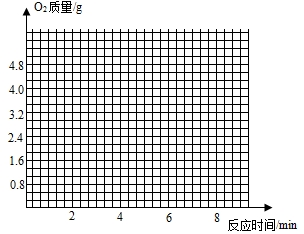 有一黑紫色的固体为KMnO4和MnO2的混合物,为测定混合物中KMnO4的质量分数,某同学取样35.0g,对固体充分加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
有一黑紫色的固体为KMnO4和MnO2的混合物,为测定混合物中KMnO4的质量分数,某同学取样35.0g,对固体充分加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):