题目内容
4.某混合物中只含有Na2SO4、Na2S和Na2SO3,硫元素的质量分数为32%,则氧元素的质量分数是( )| A. | 16% | B. | 22% | C. | 32% | D. | 46% |
分析 根据所给物质的化学式进行分析,可以发现,在这三种物质中,钠元素与硫元素的原子个数比为2:1,也就是钠元素和硫元素的质量比是定值,从而确定氧元素的质量分数.
解答 解:在这三种物质中,钠元素与硫元素的原子个数比为2:1,也就是钠元素和硫元素的质量比是定值:46:32,所以若硫元素的质量分数为32%,则钠元素的质量分数是46%,故氧元素的质量分数为:1-46%-32%=22%,
故选B.
点评 本题考查了混合物中某元素质量分数的求算,完成此题,可以依据物质中元素的固定质量比进行.

练习册系列答案
相关题目
15.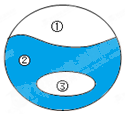 如图为物质的分类关系,①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )
如图为物质的分类关系,①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )
 如图为物质的分类关系,①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )
如图为物质的分类关系,①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )| A. | 一氧化碳 | B. | 硫酸铜晶体 | C. | 空气 | D. | 铜 |
12.作为相对原子质量标准的碳-12可以写成${\;}_{\;}^{12}$C,1个${\;}_{\;}^{12}$C的原子的质量为a千克,1个${\;}_{\;}^{12}$CO2分子的质 量为b千克,若以12CO2分子中的1个氧原子质量的$\frac{1}{16}$作为相对原子质量的标准,则12CO2的相对分子质量是( )
| A. | $\frac{32b}{b-a}$ | B. | $\frac{32b}{a-b}$ | C. | $\frac{16b}{b-a}$ | D. | $\frac{8b}{b-a}$ |
19. 向甲物质中逐渐加入乙物质至过量.若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )
向甲物质中逐渐加入乙物质至过量.若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )
 向甲物质中逐渐加入乙物质至过量.若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )
向甲物质中逐渐加入乙物质至过量.若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )| 选项 | 甲物质 | 乙物质 | y轴表示的含义 |
| A | 二氧化锰 | 过氧化氢溶液 | 二氧化锰的质量 |
| B | 不饱和蔗糖水 | 加水 | 溶质的质量 |
| C | t℃的水 | 氢氧化钠固体 | 氢氧化钠的溶解度 |
| D | 饱和食盐溶液 | 恒温蒸发溶剂 | 溶液质量分数 |
| A. | A | B. | B | C. | C | D. | D |
13.某无色溶液中所含离子的个数比为K+:H+:SO42-:OH-:Cl-=2n:x:n:y:n,则此溶液的pH( )
| A. | >7 | B. | <7 | C. | =7 | D. | 无法确定 |
10.某溶液中可能含有以下离子中的若干种:Na+、NH4+、Ba2+、Cl-、CO32-、SO42-.现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体0.68g;②第二份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.根据上述实验,以下推测正确的是( )
| A. | 一定不存在Ba2+,NH4+可能存在 | B. | CO32-一定存在 | ||
| C. | 可能存在Na+ | D. | 一定不存在Cl- |
11.在一定条件下,同一反应进行的快慢与反应物的质量分数成正比.现用100克、溶质的质量分数为30%的硫酸溶液与过量镁粉反应,为了使反应不致太快而又不影响生成氢气的总量,可向所用的硫酸中加入适量的( )
| A. | NaOH溶液 | B. | CuSO4溶液 | C. | K2SO4溶液 | D. | Na2CO3溶液 |