题目内容
13.某无色溶液中所含离子的个数比为K+:H+:SO42-:OH-:Cl-=2n:x:n:y:n,则此溶液的pH( )| A. | >7 | B. | <7 | C. | =7 | D. | 无法确定 |
分析 根据中和反应的实质H++OH-═H2O分析.
解答 解:中和反应的实质是H++OH-═H2O,H+与OH-的个数比1:1反应,由于H+:OH-=x:y,所以无法确定哪种离子过量,无法确定无色溶液pH的情况.
故选:D.
点评 酸性溶液的pH值<7;中性溶液的pH值=7;碱性溶液的pH值>7.

练习册系列答案
相关题目
4.某混合物中只含有Na2SO4、Na2S和Na2SO3,硫元素的质量分数为32%,则氧元素的质量分数是( )
| A. | 16% | B. | 22% | C. | 32% | D. | 46% |
9.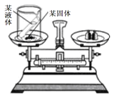 某科学兴趣小组的同学利用如图所示实验装置验证质量守恒定律. 则小试管中的液体和烧杯中的固体应分别选用( )
某科学兴趣小组的同学利用如图所示实验装置验证质量守恒定律. 则小试管中的液体和烧杯中的固体应分别选用( )
 某科学兴趣小组的同学利用如图所示实验装置验证质量守恒定律. 则小试管中的液体和烧杯中的固体应分别选用( )
某科学兴趣小组的同学利用如图所示实验装置验证质量守恒定律. 则小试管中的液体和烧杯中的固体应分别选用( )| A. | 水和氯化钠固体 | B. | 氢氧化钙溶液和碳酸钠粉末 | ||
| C. | 稀盐酸和铁粉 | D. | 5%双氧水和二氧化锰粉末 |
5.下列除去杂质的方法正确的是( )
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | 二氧化锰 | 氯化钠 | 加水溶解,过滤,蒸发结晶 |
| B | 氯化钠溶液 | 碳酸钠 | 加入过量稀盐酸,加热蒸发 |
| C | 氯化钙溶液 | 稀盐酸 | 加入过量氢氧化钙,过滤 |
| D | 氢氧化钠溶液 | 碳酸钠 | 加入适量的石灰水 |
| A. | A | B. | B | C. | C | D. | D |
2.为测定一瓶氢氧化钠溶液的溶质质量分数,小明取20.0克此溶液于烧杯中,逐滴滴加溶质质量分数为7.3%的稀盐酸,并随时测得反应后溶液的pH,所得数据如下表:
试回答:
(1)当实验序号为3时,氢氧化钠与稀盐酸恰好完全反应;
(2)当滴加稀盐酸的质量为10.1克时,所得溶液中的溶质是氯化钠和氯化氢;
(3)计算所测氢氧化钠溶液中溶质的质量分数.
| 实验序号 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸的质量/克 | 9.8 | 9.9 | 10.0 | 10.1 | 10.2 |
| 溶液的pH | 12.1 | 11.8 | 7.0 | 2.2 | 1.9 |
(1)当实验序号为3时,氢氧化钠与稀盐酸恰好完全反应;
(2)当滴加稀盐酸的质量为10.1克时,所得溶液中的溶质是氯化钠和氯化氢;
(3)计算所测氢氧化钠溶液中溶质的质量分数.
3. 今年6月8日至14日是全国节能宣传周,活动主题是“携手节能低碳,共建碧水蓝天”.根据如图碳循环的部分过程进行的有关分析中,错误的是( )
今年6月8日至14日是全国节能宣传周,活动主题是“携手节能低碳,共建碧水蓝天”.根据如图碳循环的部分过程进行的有关分析中,错误的是( )
 今年6月8日至14日是全国节能宣传周,活动主题是“携手节能低碳,共建碧水蓝天”.根据如图碳循环的部分过程进行的有关分析中,错误的是( )
今年6月8日至14日是全国节能宣传周,活动主题是“携手节能低碳,共建碧水蓝天”.根据如图碳循环的部分过程进行的有关分析中,错误的是( )| A. | ②是指生产者、消费者和分解者的呼吸作用 | |
| B. | 在生物群落的食物链中,碳是以二氧化碳的形式进行传递的 | |
| C. | 在城市交通中少开汽车多骑自行车能减少①过程的发生 | |
| D. | 绿化环境、爱护草木有利于③过程的进行 |

