题目内容
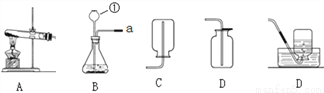
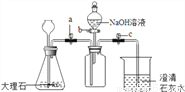
除杂是化学实验的重要环节,下列实验方法能达到实验目的是
实验目的 | 实验方法 | |
A. | 除去CO中混有的少量H2O、CO2 | 依次通过浓硫酸、氢氧化钠溶液 |
B. | 除去N2中混有的O2 | 将气体通过灼热的铜粉 |
C. | 除去KCl中混有的MnO2 | 加足量水溶解,过滤、洗涤、干燥 |
D. | 除去KNO3溶液中混有的K2CO3 | 加入适量稀硝酸,充分反应后,蒸发结晶 |
A. A B. B C. C D. D
B 【解析】除杂的原则:只除杂,不引杂。即所加试剂只能与杂质反应,不能与想要的主要成分反应,同时不能引入新的杂质。A、浓硫酸能除去二氧化碳中的水蒸气,氢氧化钠溶液能除掉二氧化碳,但是经过溶液后的一氧化碳中又会引入水蒸气,错误;B、加热条件下,铜和氧气反应生成固体氧化铜,氮气不反应,能成功除杂,正确;C、氯化钾易溶于水,二氧化锰难溶于水,除去KCl中混有的MnO2,应加足量水溶解,过滤,将溶液...
练习册系列答案
相关题目