题目内容
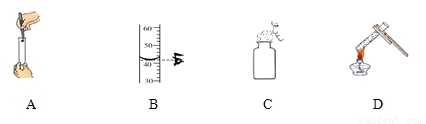
我们已经学习过实验室制取一些气体的反应原理、发生装置及收集方法,请根据下列实验装置图回答问题:
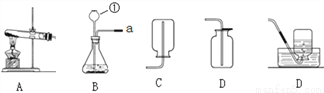

(1)写出装置图中标号仪器的名称:①_________。
(2)如选用装置A作为制取氧气的发生装置,其化学方程式可以为_________________。
(3)实验室使用稀盐酸和金属锌制取氢气的化学反应方程式为__________________,这种方法制得的氢气往往含有少量杂质气体,若用B、E、F等装置制取并收集纯净的氢气,则装置的接口顺序为:a→(____) (____) →(____) (____) →收集,其中E中所放的药品为 ________ 。
(4)为了验证二氧化碳与氢氧化钠可以发生化学反应,某小组用下图所示装置进行实验。请回答下列问题:
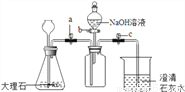
①打开止水夹a和c,关闭活塞b,从长颈漏斗向锥形瓶中注入稀盐酸,使长颈漏斗下端管口浸没在液面下的原因是___________________ 。
②当观察_______ (填实验现象)时,说明集气瓶中已集满二氧化碳气体。再向集气瓶中加入适量的NaOH溶液后,关闭活塞a、b,轻轻振 荡集气瓶。一段时间后可观察到___________ ,证明二氧化碳与氢氧化钠发生了化学反应。二氧化碳与氢氧化钠反应的化学方程式为:______________ 。
③有同学认为仅做上述实验不严密,应利用上图装置做一个对比实验。该对比实验所选的试剂是 _________ ,产生的现象与上述实验不同的是 ______________________ 。
长颈漏斗 2KMnO4K2MnO4+MnO2+O2↑ Zn+2HCl==ZnCl2+H2↑ e d b c 浓硫酸 防止气体从漏斗口逸出 澄清石灰水变浑浊 烧杯内的液体流入集气瓶内 2NaOH+CO2===Na2CO3+H2O 水(H2O) 倒吸入集气瓶中的液体的体积不同 【解析】(1)装置图中标号仪器的名称:①长颈漏斗;(2)高锰酸钾法制氧气选用装置A作为发生装置,其化学方程式可以为2KM... 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案除杂是化学实验的重要环节,下列实验方法能达到实验目的是
实验目的 | 实验方法 | |
A. | 除去CO中混有的少量H2O、CO2 | 依次通过浓硫酸、氢氧化钠溶液 |
B. | 除去N2中混有的O2 | 将气体通过灼热的铜粉 |
C. | 除去KCl中混有的MnO2 | 加足量水溶解,过滤、洗涤、干燥 |
D. | 除去KNO3溶液中混有的K2CO3 | 加入适量稀硝酸,充分反应后,蒸发结晶 |
A. A B. B C. C D. D
B 【解析】除杂的原则:只除杂,不引杂。即所加试剂只能与杂质反应,不能与想要的主要成分反应,同时不能引入新的杂质。A、浓硫酸能除去二氧化碳中的水蒸气,氢氧化钠溶液能除掉二氧化碳,但是经过溶液后的一氧化碳中又会引入水蒸气,错误;B、加热条件下,铜和氧气反应生成固体氧化铜,氮气不反应,能成功除杂,正确;C、氯化钾易溶于水,二氧化锰难溶于水,除去KCl中混有的MnO2,应加足量水溶解,过滤,将溶液...在一个密闭容器中放入A、B、M、Q四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,下列说法中,不正确的是( )
物质 | A | B | M | Q |
反应前质量(g) | 18 | 1 | 32 | 2 |
反应后质量(g) | X(未知) | 26 | 12 | 2 |
A. 反应后物质A的质量为13g
B. 该变化的基本反应类型是分解反应
C. 反应中B、M的质量比为5∶4
D. 物质Q不一定是该反应的催化剂
B 【解析】A、根据质量守恒,反应后A的质量=18g+1g+32g+2g-x+26g+12g+2g=13g,正确;B、由表格信息可知:反应后B质量增加了(26g-1g)=25g,是生成物;M质量减少了(32g-20g)=20g,是反应物;Q质量不变,可能做催化剂,可能没有参加反应;反应后A的质量=18g+1g+32g+2g-x+26g+12g+2g=13g,反应后A减少了(18g-13g)=...


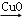 CO2 → H2CO3
CO2 → H2CO3 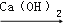 CaCO3
CaCO3  CO2
CO2