题目内容
2.燃烧、缓慢氧化、自燃的相同点是( )①都发光②都放热③都需要达到着火点④都很剧烈⑤都属于氧化反应.
| A. | ①②⑤ | B. | ②③⑤ | C. | ②③④⑤ | D. | ②⑤ |
分析 燃烧是指可燃物跟空气中的氧气发生的发光、发热的比较剧烈的氧化反应;有些氧化反应进行的比较缓慢,甚至不溶易被察觉,这样的氧化称为缓慢氧化;由缓慢氧化引起的自发燃烧叫自燃.它们的共同点是:都是氧化反应,都能放出热量.
解答 解:A、缓慢氧化不发光,故选项错误;
B、缓慢氧化不需要达到着火点,故选项错误;
C、缓慢氧化不剧烈,也不需要达到着火点,故选项错误;
D、它们的共同点是:都是氧化反应,都能放出热量.故选项正确;
故选D.
点评 本考点考查了燃烧、爆炸、缓慢氧化和自燃的关系,要加强记忆它们的概念,相同点和不同点,在理解和比较的基础上进行应用.本考点的基础性强,主要出现在选择题和填空题中.

练习册系列答案
相关题目
12.在双氧水制氧气的反应中,下列说法正确的是( )
| A. | 反应前液体中氧原子的物质的量与反应后液体中氧原子的物质的量相等 | |
| B. | 该反应属于化合反应 | |
| C. | 反应中消耗的过氧化氢中氧元素的质量就等于生成的氧气的质量 | |
| D. | 反应前液体的质量减去反应后液体的质量就等于生成的氧气的质量 |
7.下列物质中,能使溶液中的石蕊变红的是( )
| A. | 二氧化碳 | B. | 酒精 | C. | 甲醇 | D. | 醋酸 |
11.下列关于分子和原子的叙述正确的是( )
| A. | 物质只能由分子或原子构成 | |
| B. | 原子核都由质子和中子构成 | |
| C. | 化学变化前后,分子种类改变,原子种类不变 | |
| D. | 两种不同种元素的原子只能构成一种分子 |
12.下列物质中属于纯净物的是( )
| A. |  酸奶 | B. |  加碘食盐 | C. |  白醋 | D. |  干冰(固态CO2) |
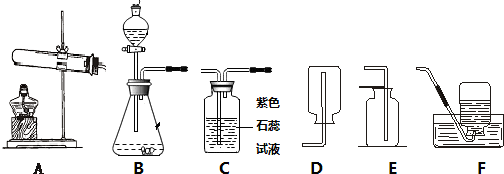
 某同学用如图方法用红磷测定空气中氧气的含量的实验,实验步骤如下:
某同学用如图方法用红磷测定空气中氧气的含量的实验,实验步骤如下: 示,请回答下列问题.
示,请回答下列问题.