题目内容
把适量的稀盐酸倒入盛有过量铁粉和少量氧化铜的试管里微热后,静置片刻后过滤,滤纸上留下什么物质?滤液里有什么物质?
答案:
解析:
解析:
|
答案:滤纸上留下的物质是铁和铜;滤液中含有的物质是氯化亚铁. 点拨:稀盐酸倒入盛有过量铁粉和少量氧化铜的试管里会发生如下反应: Fe+2HCl CuO+2HCl 因为铁粉过量,过量的铁粉又与氯化铜发生置换反应:Fe+CuCl2 |

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
中考前复习,小芳打算把厨房中盛有淀粉、NaCl、Na2CO3、NaHCO3的调料盒贴上标签.中考结束帮妈妈做家务.请你帮助小芳完成如下探究过程:
实验准备工作:将四种调料盒编号为A、B、C、D
(1)取四种白色固体各少量于试管中,加适量水充分振荡.通过实验将B盒贴上写有 的标签
(2)取A、C、D各少量于试管中,实验记录如下,填齐下表:
编号A的调料盒为
(3)查阅资料:
资料1:碳酸钠和碳酸氢钠在一定条件下可以相互转化,转化过程如图所示:
NaHCO3
Na2CO3
资料2:
(4)依据资料,帮助小芳完成如下实验方案设计来区别NaHCO3和Na2CO3:
实验方案1:小芳拟定用如图所示装置进行实验,若洁净试管中的物质为碳酸氢钠,小芳观察到的现象有 .
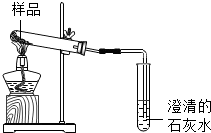
实验方案2:取两种待检测样品制成20°C的饱和溶液,取两种饱和溶液适量分别于试管中,向试管中通入二氧化碳, (写出实验现象和对应结论).
实验方案3:设计下列实验请填现象和结论
实验准备工作:将四种调料盒编号为A、B、C、D
(1)取四种白色固体各少量于试管中,加适量水充分振荡.通过实验将B盒贴上写有
(2)取A、C、D各少量于试管中,实验记录如下,填齐下表:
| 样品 实验现象 所加试剂 |
A | C | D |
| 无现象 | 有气泡 |
(3)查阅资料:
资料1:碳酸钠和碳酸氢钠在一定条件下可以相互转化,转化过程如图所示:
NaHCO3
| △ |
| H2O、CO2 |
资料2:
| 温度 溶解度 盐 |
10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
实验方案1:小芳拟定用如图所示装置进行实验,若洁净试管中的物质为碳酸氢钠,小芳观察到的现象有

实验方案2:取两种待检测样品制成20°C的饱和溶液,取两种饱和溶液适量分别于试管中,向试管中通入二氧化碳,
实验方案3:设计下列实验请填现象和结论
| 实验操作 | 实验现象 | 结论 |
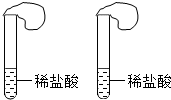 两个试管各加足量且相等的稀盐酸, 试管上系的气球里各装入106克 两种白色粉末,同时倒入盐酸中. |
中考前复习,小芳打算把厨房中盛有淀粉、NaCl、Na2CO3、NaHCO3的调料盒贴上标签。中考结束帮妈妈做家务。请你帮助小芳完成如下探究过程:
实验准备工作:将四种调料盒编号为A、B、C、D
(1)取四种白色固体各少量于试管中,加适量水充分振荡。通过实验将B盒贴上写有 的标签
(2)取A、C、D各少量于试管中,实验记录如下,填齐下表:
编号A的调料盒为
(3)查阅资料:
资料1:碳酸钠和碳酸氢钠在一定条件下可以相互转化,转化过程如下图所示:
资料2: (4)依据资料,帮助小芳完成如下实验方案设计来区别NaHCO3和Na2CO3:
(4)依据资料,帮助小芳完成如下实验方案设计来区别NaHCO3和Na2CO3:
实验方案1:小芳拟定用如图所示装置进行实验,若洁净试管中的物质为碳酸氢钠,小芳观察到的现象有 。
实验方案2:取两种待检测样品制成20oC的饱和溶液,取两种饱和溶液适量分别于试管中,向试管中通入二氧化碳, (写出实验现象和对应结论)。
实验方案3:设计下列实验请填现象和结论
| 实验操作 | 实验现象 | 结论 |
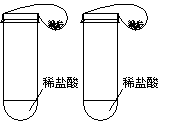 两个试管各加足量且相等的稀盐酸,试管上系的气球里各装入106克 两种白色粉末,同时倒入盐酸中。 | | |