题目内容
19.小华利用溶液导电性进行实验设计方案进行探究NaOH和盐酸的反应.分别测定几种试剂的导电性,获得相关数据:
| 实验序号 | A | B | C | D |
| 试剂 | 蒸馏水 | 稀盐酸 | NaOH溶液 | NaCl溶液 |
| 电流强度/mA | 约为0 | 0.09 | 0.09 | 0.09 |
I.溶液中若存在自由移动的离子,通电时就会发生定向移动,从而形成了电流.
II.相同电压下,等体积溶液中,所含离子数目越多,电流就越大.
①对比实验A、C的数据,可推知NaOH溶液中除水分子外还含有自由移动的Na+和OH-(填化学符号).
②实验B、D中电流强度相等,说明等体积的稀盐酸和NaCl溶液中所含Cl-的数目相等(填写“相等”或“不相等”).
③各取10mL NaOH溶液于两个小烧杯中,分别加入10mL NaCl溶液和10mL稀盐酸(所得混合溶液体积均约为20mL),测两种混合溶液的导电性,电流示数依次为I1和I2.根据I1> I2(填“>”、“<”或“=”),也可推断氢氧化钠和盐酸发生了反应.
分析 ①NaOH溶液中除水分子外还含有自由移动的钠离子和氯离子;
②电流强度与离子浓度成正比来分析;
③氢氧化钠与盐酸反应生成水,使溶液中离子减少来分析
解答 解:①NaOH溶液中除水分子外还含有自由移动的钠离子和氢氧根离子;
②电流强度与离子浓度有关,实验B、D中电流强度相等,说明等体积的稀盐酸和NaCl溶液中所含Cl-的数目相等;
③氢氧化钠氢氧根离子与盐酸中的氢离子反应生成水,使溶液中离子减少;而 NaOH溶液与氯化钠溶液不反应离子不减少,故I1大于I2.
故答案为:①Na+和OH-;②相等;③>.
点评 结合课本知识和实验技能,考查了学生的分析问题、解决问题的能力;此题综合性较强,考查出学生将理论知识与实验相结合的能力,还考查学生的创新能力,是一道不错的综合题.

练习册系列答案
相关题目
7.下列符号中,只有微观意义的是( )
| A. | Fe | B. | H | C. | 2N | D. | O |
4.兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
(1)氢氧化钠固体要密封保存,原因有:
①氢氧化钠固体易潮解;②氢氧化钠与空气中二氧化碳反应变质.
【对固体猜想】
猜想一:全部是NaOH;猜想二:全部是Na2CO3;猜想三:是NaOH和Na2CO3混合物
【实验和推断】(2)为进一步确定成分,进行了以下探究:
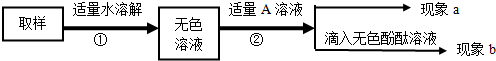
对无色溶液进行以下实验:
③分析:小组中有同学提出质疑,认为以上实验不能证明猜想三成立,理由是:第一步氢氧化钙溶液与碳酸钠溶液反应生成氢氧化钠,干扰第二步氢氧化钠的检验.
④反思:把第一步中的氢氧化钙溶液换成氯化钙溶液,可达到实验目的.
(3)请利用以下提供的试剂,设计实验证明猜想一是正确的,即氢氧化钠没有变质.
提供的试剂有:酚酞溶液、稀盐酸、氢氧化钡溶液、氯化钡溶液
(1)氢氧化钠固体要密封保存,原因有:
①氢氧化钠固体易潮解;②氢氧化钠与空气中二氧化碳反应变质.
【对固体猜想】
猜想一:全部是NaOH;猜想二:全部是Na2CO3;猜想三:是NaOH和Na2CO3混合物
【实验和推断】(2)为进一步确定成分,进行了以下探究:

对无色溶液进行以下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 第一步: 用试管取约2mL该溶液,滴入适量氢氧化钙溶液,振荡. | 现象a:白色沉淀 | 化学方程式: ①Na2CO3+Ca(OH)2=2NaOH+CaCO3↓,有碳酸钠并全部除尽. |
| 第二步: 静置,取上层清液于试管中滴入酚酞溶液,振荡. | 现象b: ②液体变红 | 含有NaOH,猜想三成立,是NaOH和Na2CO3混合物 |
④反思:把第一步中的氢氧化钙溶液换成氯化钙溶液,可达到实验目的.
(3)请利用以下提供的试剂,设计实验证明猜想一是正确的,即氢氧化钠没有变质.
提供的试剂有:酚酞溶液、稀盐酸、氢氧化钡溶液、氯化钡溶液
| 实验操作 | 实验现象 | 实验结论 |
11.日常生活中会接触到“高钙牛奶,加碘盐”,这里的钙,碘指的是( )
| A. | 单质 | B. | 原子 | C. | 元素 | D. | 离子 |
 空气、水、金属等是重要的资源
空气、水、金属等是重要的资源 ”均为铜片),只需完成实验B和D即可达到探究目的(填字母).
”均为铜片),只需完成实验B和D即可达到探究目的(填字母).

 根据图所示的装置,回答下列问题.
根据图所示的装置,回答下列问题.