题目内容
13.规范的实验操作是实验成功的前提,请回答:(1)量取8mL稀硫酸,应选用10mL的量筒.
(2)胶头滴管用过后应洗净,再去吸取其他药品.
(3)玻璃管插入带孔橡皮塞,先把玻璃管的一段用水润湿,然后稍稍用力转动插入.
(4)清洗试管时如果内壁附着的水既不聚成水滴,也不成股流下,则表示试管已洗干净.
分析 (1)根据量筒在量取液体时的选取原则分析.
(2)胶头滴管用完后,不清洗,再去吸取别的药品,会污染别的药品.
(3)了解玻璃管插入带孔橡皮塞的方法.
(4)根据实验室正确洗涤试管的方法作答.
解答 解:(1)在实验室量取液体时,因为量程太大,会使区分度增大,而加大误差;量程太小,需量取多次,也会加大误差,采用就近原则,
故答案为:10.
(2)胶头滴管用完后,洗涤干净晾干,防止污染别的药品.
故答案为:洗净.
(3)玻璃管插入带孔橡皮塞,先把玻璃管的一段用水润湿,然后稍稍用力转动插入.
故答案为:用水润湿.
(4)试管内有不宜洗掉的物质时,要用试管刷刷洗,当洗过的玻璃仪器内的水既不聚成水滴,也不成股流下时,表示仪器已洗干净.
故答案为:聚成水滴;成股流下.
点评 本题主要了解各操作的注意事项;考查常用量筒、胶头滴管的使用方法;了解仪器的装配或连接方法.

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案
相关题目
4.如图是甲、乙两种物质的溶解度曲线.下列说法中不正确的是( )


| A. | 当温度由t3→t2时,乙溶液由m→n的变化是由不饱和转化为饱和 | |
| B. | t3时同处a点的甲、乙物质的溶解度降温到t1时都会有晶体析出 | |
| C. | 要配制质量分数相等的甲、乙两种饱和溶液,温度应该控制在t2℃ | |
| D. | 当温度由t2→t1时,甲溶液由n→h的溶质质量分数可能不变 |
8.小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加.
【知识回放】金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHg Ag Pt Au,请你在横线上填写对应金属的元素符号.
【作出猜想】猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
【结论与解释】
(1)小聪得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的物质.
【知识运用】
将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4═CrSO4+Fe.
【知识回放】金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHg Ag Pt Au,请你在横线上填写对应金属的元素符号.
【作出猜想】猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 |  |  |  |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 铜片表面不产生气泡 |
(1)小聪得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的物质.
【知识运用】
将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4═CrSO4+Fe.
2.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( )
| A. | 紫色石蕊试液 | B. | 氯化钠溶液 | C. | 铜粉 | D. | 氧化铜粉末 |
 用如图所示的装置制氧气并测定收集氧气的体积.锥形瓶内盛有一定量的二氧化锰和适量的过氧化氢溶液,B中盛满水,请根据实验回答下列问题:
用如图所示的装置制氧气并测定收集氧气的体积.锥形瓶内盛有一定量的二氧化锰和适量的过氧化氢溶液,B中盛满水,请根据实验回答下列问题: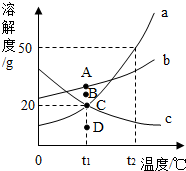 如图所示是固体a、b、c三种物质的溶解度随温度变化的曲线图,根据图示回答:
如图所示是固体a、b、c三种物质的溶解度随温度变化的曲线图,根据图示回答: