题目内容
实验室用含碳酸钙20g的大理石与100g的稀盐酸恰好反应,生成二氧化碳多少g?______稀盐酸的溶质质量分数是多少?______.
设生成二氧化碳的质量为x,稀盐酸中HCl的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
20g y x
=
=
x=8.8g,y=14.6g
稀盐酸的溶质质量分数=
×100%=14.6%
故答案为:8.8g;14.6%.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
20g y x
| 100 |
| 20g |
| 73 |
| y |
| 44 |
| x |
x=8.8g,y=14.6g
稀盐酸的溶质质量分数=
| 14.6g |
| 100g |
故答案为:8.8g;14.6%.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目


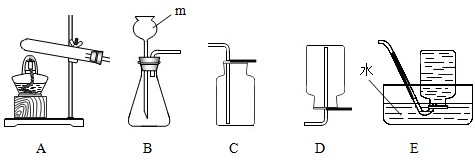
 下列是初三某合作学习小组实验室制取二氧化碳气体
下列是初三某合作学习小组实验室制取二氧化碳气体