题目内容
4.下表是Ba(OH)2 和Ca(OH)2 在不同温度下的溶解度:| 溶解度 温度 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
| Ba(OH)2 | 1.67 | 3.89 | 8.22 | 20.94 | 101.4 |
| Ca(OH)2 | 0.185 | 0.165 | 0.141 | 0.116 | 0.094 |
(2)80℃时,要使饱和的Ba(OH)2和Ca(OH)2的混合溶液结晶析出Ba(OH)2而不析出Ca(OH)2,可采取的结晶方法是降温结晶,理由是氢氧化钡的溶解度受温度影响较大,随温度的升高而增大;氢氧化钙的溶解度随温度的升高而减小.要将结晶析出的Ba(OH)2晶体与混合溶液分离开来,可采取过滤法,使用该方法实验时所需要的仪器有烧杯、漏斗、玻璃棒和铁架台.操作中,若某同学向漏斗中倾倒液体时,液面超过滤纸边缘,你认为应如何处理?将滤液再过滤.
(3)实验室有一份Ba(OH)2样品,其中含有少量Ca(OH)2杂质,现要除去其中杂质,得到纯净的Ba(OH)2,试设计一套合理的实验方案(按实验的先后顺序写简要步骤即可).
分析 (1)根据表格中的数据分析解答;
(2)根据降温结晶方法和过滤的基本操作分析解答;
(3)根据氢氧化钡和氢氧化钙溶解度随温度的变化情况和降温结晶、过滤基本操作分析设计.
解答 解:(1)由表格可知氢氧化钡的溶解度受温度的影响较大,并且溶解度随温度的升高而增大;氢氧化钙的溶解度较小,且随温度的升高而减小;故答案:
氢氧化钡的溶解度随温度的升高而增大;氢氧化钙的溶解度随温度的升高而减小;
(2)氢氧化钡的溶解度受温度的影响较大,并且溶解度随温度的升高而增大;氢氧化钙的溶解度较小,且随温度的升高而减小;所以降低温度,氢氧化钡结晶析出,然后过滤就得到氢氧化钡,过滤时要用到:烧杯、漏斗、滤纸、玻璃棒和铁架台;过滤时液面高于滤纸边缘,滤液会浑浊,要再过滤滤液;故答案:降温结晶;氢氧化钡的溶解度随温度的升高而增大;氢氧化钙的溶解度随温度的升高而减小;烧杯、漏斗、滤纸、玻璃棒和铁架台;将滤液再过滤;
(3)氢氧化钡的溶解度随温度的升高而增大;氢氧化钙的溶解度随温度的升高而减小,所以先将二者的混合物溶解在热水中制成氢氧化钡的饱和溶液,然后冷却氢氧化钡析出,氢氧化钙不会析出,过滤即可得到氢氧化钡晶体,故答案:将二者的混合物溶解在热水中制成氢氧化钡的饱和溶液然后冷却氢氧化钡析出,氢氧化钙不会析出,过滤即可得到氢氧化钡晶体.
点评 本题主要考查物质的除杂或净化问题,掌握混合物的一些分离方法,了解碳酸钠、碳酸氢钠与碳酸钙的性质.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
6.保护环境、防止污染,人人应引起重视.下列反应的生成物不会污染空气的是( )
| A. | 点燃爆竹 | B. | 燃烧煤炭 | ||
| C. | 氢气通入氧化铜后加热 | D. | 氢气在氯气中燃烧 |
10.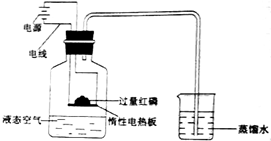 常温常压下,液态空气的沸点是-192℃,其简易获取过程:第一步:空气除尘净化,除去二氧化碳和水蒸气;第二步:在低温、高压的条件下,使空气液化,再用液态空气进行实验的装置如图:
常温常压下,液态空气的沸点是-192℃,其简易获取过程:第一步:空气除尘净化,除去二氧化碳和水蒸气;第二步:在低温、高压的条件下,使空气液化,再用液态空气进行实验的装置如图:
实验说明:电路开始处于断开状态,一旦接通电路,惰性电热板能起加热作用.
实验步骤及现象:
根据以上信息,回答下列问题:
(1)工业上制取液态空气时,常常需要将空气依次经过①液化器、②净化器、③压缩机等,你认为空气首先应经过②(选填①、②、③);
(2)请完善表格中的实验现象.
A烧杯中导管口不断产生气泡;
B导管中出现倒吸;
(3)步骤Ⅲ中,产生实验现象A的两个主要原因:①液态空气蒸腾产生大量的气体,该气体的主要成分是氮气;②装置内的压强不断增大;
(4)步骤Ⅳ中,红磷燃烧的化学符号表达式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
 常温常压下,液态空气的沸点是-192℃,其简易获取过程:第一步:空气除尘净化,除去二氧化碳和水蒸气;第二步:在低温、高压的条件下,使空气液化,再用液态空气进行实验的装置如图:
常温常压下,液态空气的沸点是-192℃,其简易获取过程:第一步:空气除尘净化,除去二氧化碳和水蒸气;第二步:在低温、高压的条件下,使空气液化,再用液态空气进行实验的装置如图:实验说明:电路开始处于断开状态,一旦接通电路,惰性电热板能起加热作用.
实验步骤及现象:
| 实验步骤 | 实验现象 |
| Ⅰ检查装置气密性,气密性良好 | -- |
| Ⅱ按装置要求连接好装置,并装好试剂 | 液态空气不断蒸腾,量不断减少,烧杯中导管口不断产生气泡 |
| Ⅲ一段时间后,接通电路 | 红磷不燃烧,烧杯中导管口不断产生气泡 |
| Ⅳ液态空气蒸发余下约十分之一时 | 红磷燃烧后,冒出大量白烟,放出大量热,… |
| Ⅴ红磷熄灭后,断开电路 | 白烟逐渐消失,导管中出现倒吸 |
(1)工业上制取液态空气时,常常需要将空气依次经过①液化器、②净化器、③压缩机等,你认为空气首先应经过②(选填①、②、③);
(2)请完善表格中的实验现象.
A烧杯中导管口不断产生气泡;
B导管中出现倒吸;
(3)步骤Ⅲ中,产生实验现象A的两个主要原因:①液态空气蒸腾产生大量的气体,该气体的主要成分是氮气;②装置内的压强不断增大;
(4)步骤Ⅳ中,红磷燃烧的化学符号表达式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
16.欲将100g溶质质量分数为10%的NaOH溶液变成质量分数为20%的NaOH溶液可采取的方法有( )
| A. | 加入100g 10%的NaOH溶液 | B. | 加入10g溶质 | ||
| C. | 蒸发掉45g水 | D. | 加入12.5g溶质 |
14.我市属于酸雨污染程度较重的地区(pH值小于5.65的酸性降水叫酸雨),据兰溪市气象站监测显示:2010年3月19日、20日、21日我市降雨的PH值分别为4.2、3.52和4.11.
(1)从数据看,2010年3月19日、20日、21日的降雨是酸雨.(填“是”或“不是”)
(2)长期酸雨会改变土壤的酸碱度,从而影响农作物的生长.参照下表,从土壤的酸碱性考虑,在我们兰溪最不适宜种植的作物是甘草
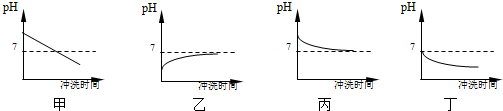
(3)农民若引接近中性的淡水冲洗土壤以降低其酸性,下列甲、乙、丙和丁四幅图中,符合冲洗过程土壤PH变化的曲线是乙
(1)从数据看,2010年3月19日、20日、21日的降雨是酸雨.(填“是”或“不是”)
(2)长期酸雨会改变土壤的酸碱度,从而影响农作物的生长.参照下表,从土壤的酸碱性考虑,在我们兰溪最不适宜种植的作物是甘草
| 作 物 | 茶 | 油菜 | 西瓜 | 甘草 |
| 最适宜的pH范围 | 4.5-5.5 | 5.8-6.7 | 6.0-7.0 | 7.2-8.5 |

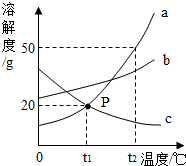 如图是a.、b、c三种物质(均不含结晶水)的溶解度曲线,请你回答:
如图是a.、b、c三种物质(均不含结晶水)的溶解度曲线,请你回答: