题目内容
7. 在学习“金属的冶炼”时,某学习小组用如图所示的装置测量氧化铜样品中氧化铜的质量分数,实验所取氧化铜样品质量为10克.(所含杂质不参加反应)
在学习“金属的冶炼”时,某学习小组用如图所示的装置测量氧化铜样品中氧化铜的质量分数,实验所取氧化铜样品质量为10克.(所含杂质不参加反应)(1)该实验利用了一氧化碳的还原性,玻璃管内观察到的现象是黑色粉末变成红色;
(2)甲同学的方法:先测出氢氧化钠溶液的质量为50克,待反应完全后再次称量,质量为54.4克,请你计算样品中氧化铜的质量分数.(一氧化碳不与氢氧化钠溶液反应)
(3)乙同学的方法:先称量出玻璃管及样品的总质量为m1,待反应完全后再次称量,质量为m2,利用m1-m2的值,求出样品中氧化铜的质量分数,其中m1-m2的值是指氧元素的质量;
(4)同学们查阅到CO除了具有可燃性、难溶于水等性质外,还具有有毒性,因此,本实验中还需对尾气进行处理,请你提出一种处理方法将尾气点燃.
分析 (1)根据一氧化碳具有还原性,可以将金属氧化物还原成金属,一氧化碳和氧化铜加热生成氧化铜是二氧化碳进行分析;
(2)根据氢氧化钠会与二氧化碳反应,氢氧化钠溶液增加的质量就是二氧化碳的质量,然后依据化学方程式求出氧化铜的质量;
(3)根据质量守恒定律进行分析;
(4)根据一氧化碳具有可燃性进行分析.
解答 解:(1)一氧化碳具有还原性,可以将金属氧化物还原成金属,一氧化碳和氧化铜加热生成氧化铜是二氧化碳,所以玻璃管内观察到的现象是:黑色粉末变成红色;
(2)生成二氧化碳的质量为:54.4g-50g=4.4g,
设样品中氧化铜的质量为x,
CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$CO2+Cu
80 44
x 4.4g
$\frac{80}{x}$=$\frac{44}{4.4g}$
x=8g
$\frac{8g}{10g}$×100%=80%;
(3)化学反应前后原子个数不变,所以先称量出玻璃管及样品的总质量为m1,待反应完全后再次称量,质量为m2,利用m1-m2的值,求出样品中氧化铜的质量分数,其中m1-m2的值是指氧元素的质量;
(4)一氧化碳具有可燃性,可以将一氧化碳进行点燃处理.
故答案为:(1)还原性,黑色粉末变成红色;(2)80%;(3)氧元素;(4)将尾气点燃.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
17.下列课题侧重于化学学科研究领域的是( )
| A. | 计算机软件的开发 | |
| B. | “神七”飞船从地球轨道转到月球轨道 | |
| C. | 利用指南针确定航海方向 | |
| D. | 新型可降解塑料袋的研制 |
15.鉴别物质的方法错误的是( )
| A. | 用酚酞鉴别食盐水和稀醋酸 | B. | 用水鉴别生石灰和石灰石 | ||
| C. | 用燃着的木条鉴别空气和二氧化碳 | D. | 用氯化钡溶液鉴别稀盐酸和稀硫酸 |
2.某同学去我市石门县壶瓶山风景区游玩,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,他称取12g样品,将60g稀盐酸分四次加入,测量的有关数据如表(已知样品中的杂质不溶于水,且不与稀盐酸反应).求:
(1)样品中碳酸钙的质量分数;
(2)所用稀盐酸的溶质质量分数?
(3)继续加入石灰石直到稀盐酸全部反应完过滤所得滤液的溶质质量分数为多少?
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量(g) | 15.0 | 15.0 | 15.0 | 15.0 |
| 剩余固体的质量(g) | 8.0 | 4.0 | 2.0 | 2.0 |
(2)所用稀盐酸的溶质质量分数?
(3)继续加入石灰石直到稀盐酸全部反应完过滤所得滤液的溶质质量分数为多少?
12.法拉第曾以《蜡烛的故事》为题为青少年连续开展了多次报告.下列列举了报告中涉及的问题及对问题的回答,其中“对问题的回答”属于“设计实验方案”的是( )
| 选项 | 问题 | 对问题的回答 |
| A | 吹灭蜡烛时产生的白烟是什么? | 主要成分是烛油蒸气 |
| B | 火焰为什么向上? | 热气流上升,形成对流 |
| C | 火焰明亮的原因是什么? | 与火焰中有碳颗粒有关,碳颗粒会影响火焰明亮程度 |
| D | 火焰不同部位温度高低如何比较? | 用一张纸在火焰中心一掠,观察纸上留下的火痕特点 |
| A. | A | B. | B | C. | C | D. | D |
16.下列物质的用途是利用物质化学性质的是( )
| A. | 干冰--作致冷剂 | B. | 小苏打--焙制制糕点的发酵剂 | ||
| C. | 汽油--洗涤衣物上的油迹 | D. | 合金钢--制造坦克外壳 |
17. 工业上用甲和乙反应制备燃料丙.根据下列微观示意图得出的结论中,正确的是( )
工业上用甲和乙反应制备燃料丙.根据下列微观示意图得出的结论中,正确的是( )
 工业上用甲和乙反应制备燃料丙.根据下列微观示意图得出的结论中,正确的是( )
工业上用甲和乙反应制备燃料丙.根据下列微观示意图得出的结论中,正确的是( )| A. | 甲中碳、氢元素的质量比为1:2 | |
| B. | 反应中甲、乙、丙的分子个数比为2:1:1 | |
| C. | 丙中质量分数最大的是碳元素 | |
| D. | 甲、乙、丙都含有碳元素和氢元素 |
 (1)X、Y、Z、W、R是初中化学常见的五种元素,X的单质是密度最小的气体,Y的一种单质是天然存在的最硬物质,Z是地壳中含量最多的元素,W的原子序数为11,R的原子结构示意图为
(1)X、Y、Z、W、R是初中化学常见的五种元素,X的单质是密度最小的气体,Y的一种单质是天然存在的最硬物质,Z是地壳中含量最多的元素,W的原子序数为11,R的原子结构示意图为 ,请回答下列问题:①X阳离子的离子结构示意图为
,请回答下列问题:①X阳离子的离子结构示意图为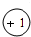 ,W离子的离子符号为Na+;
,W离子的离子符号为Na+; 用化学符号填空.
用化学符号填空.