题目内容
2.已知某原子的实际质量为Mg,又知C-12原子的质量为Ng,该原子的中子数是P,则该原子的核外电子数为( )| A. | 12M+P | B. | 12N+P | C. | $\frac{12M}{N}$+P | D. | $\frac{12M}{N}$-P |
分析 根据某原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$,结合原子中:核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数,进行分析解答即可.
解答 解:已知某原子的实际质量为Mg,又知C-12原子的质量为Ng,则该原子的相对原子质量为$\frac{Mg}{Ng×\frac{1}{12}}$=$\frac{12M}{N}$,该原子的中子数是P,由相对原子质量=质子数+中子数,则其核内质子数为$\frac{12M}{N}$-P;原子中:核电荷数=核内质子数=核外电子数,则该原子的核外电子数为$\frac{12M}{N}$-P.
故选:D.
点评 本题难度不大,掌握原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$、原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数并能灵活运用是正确解答本题的关键.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
13.下列图象与对应的叙述相符合的是( )
| A. |  向一定量的硫酸溶液中滴加氢氧化钠溶液 | |
| B. |  等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应 | |
| C. |  向一定量的稀硫酸中不断加锌粉 | |
| D. |  向H2SO4和MgSO4的混合溶液中滴加NaOH溶液 |
10.实验设计的严密性、操作的规范性等都很重要,每一个环节都会影响实验结果.
(1)研究酶的催化作用可能会受到重金属离子的影响.小柯设计如下探究:取试管3支,编号,按下表分别加入试剂,摇匀,迅速置于37℃的水浴中,10分钟后取出,冷却后分别加入碘液3滴,观察其颜色变化.
在看了小柯的设计及实验后,同桌的小温认为凭上述实验还不足以证明小柯的猜想.小温提出应该将实验中的CuSO4溶液更换成CuCl2溶液 才更有说服力.如果你也同小温一起探究,你还可以建议小柯做怎样的更换?将NaCl溶液换成Na2SO4溶液;.
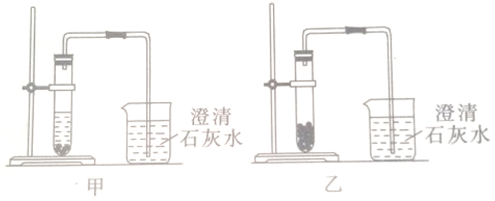
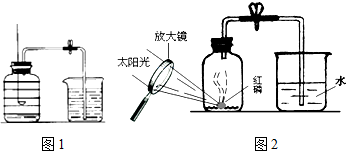
(2)小柯同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体积分数明显小于$\frac{1}{5}$.他们对课本上的实验装置进行了图2所示的改进(其他仪器忽略).小温同学提出应把图2红磷换为白磷,理由是白磷的着火点比红磷低,容易被点燃.
(3)小柯用如图3装置实验,在烧瓶底部放入MnO2,打开分液漏斗注入双氧水,烧瓶内立刻产生大量气泡,过一会儿发现打开活塞的分液漏斗内的液体静止了片刻漏斗末端出水不畅,请你解释原因烧瓶内双氧水分解快,瓶内气压大导致.

(1)研究酶的催化作用可能会受到重金属离子的影响.小柯设计如下探究:取试管3支,编号,按下表分别加入试剂,摇匀,迅速置于37℃的水浴中,10分钟后取出,冷却后分别加入碘液3滴,观察其颜色变化.
| 编号 | 0.25%淀粉溶液(ml) | 蒸馏水(ml) | 1%NaCl 溶液(ml) | 1%CuSO4 溶液(ml) | 唾液溶液(ml) | 加入碘液3滴后现象 |
| 1 | 3 | 1 | - | - | 1 | 不变蓝 |
| 2 | 3 | - | 1 | - | 1 | 不变蓝 |
| 3 | 3 | - | - | 1 | 1 | 变蓝色 |
(2)小柯同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体积分数明显小于$\frac{1}{5}$.他们对课本上的实验装置进行了图2所示的改进(其他仪器忽略).小温同学提出应把图2红磷换为白磷,理由是白磷的着火点比红磷低,容易被点燃.
(3)小柯用如图3装置实验,在烧瓶底部放入MnO2,打开分液漏斗注入双氧水,烧瓶内立刻产生大量气泡,过一会儿发现打开活塞的分液漏斗内的液体静止了片刻漏斗末端出水不畅,请你解释原因烧瓶内双氧水分解快,瓶内气压大导致.

11.某化学研究小组进行研究性学习,请你协助完成相关任务.
【研究课题1】探究水壶内部水垢的主要成分
【查阅资料】(1)天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).天然水和水垢所含的物质及其溶解性如下表:
【提出猜想】水垢的主要成分一定含有Mg(OH)2和CaCO3,可能含有Ca(OH)2和MgCO3.
【设计方案】
(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,静置.取上层清液滴入Na2CO3溶液,如果没有白色沉淀,说明水垢中无Ca(OH)2(填化学式).
(2)乙同学设计了如图2实验装置,进一步确定水垢中含有碳酸盐的成分.

其主要实验步骤如下:
①按图1组装仪器,将50g水垢试样放入锥形瓶中,逐滴加入足量稀盐酸.
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气,使装置内的气体缓缓通过后面的装置.
③称量D瓶内物质增加的质量;
④重复②和③的操作,直至D瓶内物质质量不变.
测量滴加稀盐酸体积与D瓶内物质增加质量的关系如图3曲线所示;
【思考与评价】(1)当水中含较多可溶性钙、镁化合物的水叫硬水,生活中降低水的硬度的常用方法是:煮沸
(2)A瓶中的NaOH溶液作用是吸收空气中的二氧化碳
(3)若50g水垢全部是碳酸钙,则最终应该产生二氧化碳的质量是22克
(4)一般情况下,两种不同金属形成的碳酸盐与足量盐酸反应时,若两金属的化合价相同、两种盐的质量相同,则相对分子质量小者放出的气体多.
分析曲线图可知:水垢中一定含有MgCO3(化学式)理由是:水垢中只有碳酸钙时只生二氧化碳质量是22克,实际生成CO2的质量是24g,大于22g,所以水垢中一定含有碳酸镁.
【研究课题1】探究水壶内部水垢的主要成分
【查阅资料】(1)天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).天然水和水垢所含的物质及其溶解性如下表:
| 物 质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3[来源:] |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
【设计方案】
(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,静置.取上层清液滴入Na2CO3溶液,如果没有白色沉淀,说明水垢中无Ca(OH)2(填化学式).
(2)乙同学设计了如图2实验装置,进一步确定水垢中含有碳酸盐的成分.

其主要实验步骤如下:
①按图1组装仪器,将50g水垢试样放入锥形瓶中,逐滴加入足量稀盐酸.
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气,使装置内的气体缓缓通过后面的装置.
③称量D瓶内物质增加的质量;
④重复②和③的操作,直至D瓶内物质质量不变.
测量滴加稀盐酸体积与D瓶内物质增加质量的关系如图3曲线所示;
【思考与评价】(1)当水中含较多可溶性钙、镁化合物的水叫硬水,生活中降低水的硬度的常用方法是:煮沸
(2)A瓶中的NaOH溶液作用是吸收空气中的二氧化碳
(3)若50g水垢全部是碳酸钙,则最终应该产生二氧化碳的质量是22克
(4)一般情况下,两种不同金属形成的碳酸盐与足量盐酸反应时,若两金属的化合价相同、两种盐的质量相同,则相对分子质量小者放出的气体多.
分析曲线图可知:水垢中一定含有MgCO3(化学式)理由是:水垢中只有碳酸钙时只生二氧化碳质量是22克,实际生成CO2的质量是24g,大于22g,所以水垢中一定含有碳酸镁.
12.下列物质中,最理想的能源是( )
| A. | 天然气 | B. | 氢气 | C. | 酒精 | D. | 汽油 |
 蛋白质是构成细胞的基本物质,由多种氨基酸构成,是复杂的相对分子质量巨大的物质.α-丙氨酸是组成人体蛋白质的氨基酸之一,如图是α-丙氨酸的分子结构模型图,据此回答:
蛋白质是构成细胞的基本物质,由多种氨基酸构成,是复杂的相对分子质量巨大的物质.α-丙氨酸是组成人体蛋白质的氨基酸之一,如图是α-丙氨酸的分子结构模型图,据此回答: Cl-
Cl-