题目内容
20.下面是某化学兴趣小组探究废旧干电池中白色糊状物成分的过程,请帮助他们完成相应的报告.[提出问题]白色糊状物是由什么物质组成的?
[资料]干电池的白色糊状物中含有铵根离子.
[猜想]可能含有OH-、CO32-、Cl-、SO42-中的一种或几种,白色糊状物可能是淀粉.
[设计方案]小亮首先认为不能存在的离子是OH-
,因为铵根离子遇到该离子会生成氨气.为了验证其他离子的存在情况,兴趣小组设计如下实验,请你完成以下实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取糊状物少量,加足量的水,搅拌后过滤.取少量滤液于试管中,滴加硝酸钡溶液. | 无沉淀产生 | 没有SO42-和CO32-存在 |
| (2)另取第(1)不所得滤液少量,滴加少量AgNO3 溶液 | 产生白色沉淀 | 存在的离子是Cl-氯离子 |
| (3)取白色糊状物,滴加少量碘 溶液 | 出现蓝色 | 有淀粉存在 |
分析 【设计方案】铵根离子和氢氧根离子相遇会生成氨气而不能共存,
【实验操作】(1)碳酸根离子和硫酸根离子与钡离子会生成白色沉淀,
(2)根据银离子和氯离子会生成白色的氯化银沉淀的知识进行分析,
(3)根据淀粉遇碘变蓝的性质进行分析.
解答 解:【设计方案】铵根离子和氢氧根离子反应会生成氨气,故答案为:OH-,
【实验操作】(1)因为硝酸盐都溶于水,没有硫酸根离子和碳酸根离子的存在,加入硝酸钡后,就不会出现沉淀,故答案为:没有沉淀生成,
(2)经过前面的检验,只剩下氯离子,要检验氯离子,需要用硝酸银,故答案为:硝酸银,
(3)要检验淀粉的存在,需要借助碘单质,故答案为:碘.
点评 本题主要考查了运用离子检验的方法探究物质组成的及含量,难度较大,综合性强

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
11. 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行探究,
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行探究,
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?(2)固体酒精中的氢氧化钠是否变质?
【实验探究】(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论合理(填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管总加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯上层清液于两支试管中,按如图探究.
②乙组认为甲组实验不能证明清液中一定有氢氧化钠,理由是Na2CO3溶液呈碱性,也能使酚酞变红.他们另取烧杯中上层清液,加足量氯化钡溶液,充分反映后滴加酚酞溶液,酚酞溶液变红.
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是除去溶液中的Na2CO3,排除其对NaOH检验的干扰.
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC.
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行探究,
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行探究,【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?(2)固体酒精中的氢氧化钠是否变质?
【实验探究】(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论合理(填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管总加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯上层清液于两支试管中,按如图探究.
| 方案 |  |  |
| 现象 | 溶液变红 | 产生白色沉淀 |
| 结论 | 溶液中有氢氧化钠 | 溶液中有碳酸钠 |
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是除去溶液中的Na2CO3,排除其对NaOH检验的干扰.
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC.
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
5.下列物质的用途中,利用其物理性质的是( )
| A. | 氧气用于切割金属 | B. | 干冰用于人工降雨 | ||
| C. | 铁粉用作食品保鲜吸氧剂 | D. | 氢氧化铝用于治疗胃酸过多 |
9.水是化学实验中常见且用途广泛的一种物质.对下列各实验中水的主要作用的解释不合理的是( )
| A. | 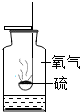 硫在氧气中燃烧--集气瓶好做水:吸收放出的热量 | |
| B. | 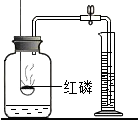 测定空气中氧气含量--量筒中的水:通过水体积变化得到氧气体积 | |
| C. |  细铁丝在氧气中燃烧--集气瓶中的水:防止集气瓶炸裂 | |
| D. | 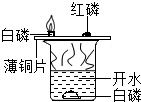 探究燃烧的条件--烧杯中的水:加热铜片:隔绝空气 |

 知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,其中b代表原子核,c代表
知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,其中b代表原子核,c代表 有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生,D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀.
有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生,D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀.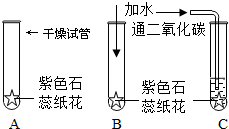 某同学设计了一套验证二氧化碳与水能否反应的实验,他首先用紫色石蕊试纸浸泡滤纸,晒干后折成纸花,然后按如图所示分别进行:
某同学设计了一套验证二氧化碳与水能否反应的实验,他首先用紫色石蕊试纸浸泡滤纸,晒干后折成纸花,然后按如图所示分别进行: