题目内容
13.托盘天平的两边各放一个盛有50mL盐酸(1mol/L)的烧杯,调节天平至平衡.现将等物质的量的甲乙两物质分别放入两烧杯中,当甲乙物质和盐酸恰好反应时,天平仍保持平衡.则甲乙可能是( )| A. | Mg和MgCO3 | B. | CaO和CaCO3 | C. | CaO和Ca(OH)2 | D. | Mg和MgO |
分析 A、1mol镁恰好和2mol稀盐酸反应生成1mol氯化镁和1mol氢气,1mol碳酸镁恰好和2mol稀盐酸反应生成1mol氯化镁、1mol水和1mol二氧化碳;
B、1mol氧化钙恰好和2mol稀盐酸反应生成1mol氯化钙和1mol水,1mol碳酸钙恰好和2mol稀盐酸反应生成1mol氯化钙、1mol水和1mol二氧化碳;
C、1mol氧化钙恰好和2mol稀盐酸反应生成1mol氯化钙和1mol水,1mol氢氧化钙恰好和2mol稀盐酸反应生成1mol氯化钙和2mol水;
D、1mol镁恰好和2mol稀盐酸反应生成1mol氯化镁和1mol氢气,1mol氧化镁恰好和2mol稀盐酸反应生成1mol氯化镁和1mol水.
解答 解:A、当镁、碳酸镁和盐酸恰好反应时,消耗的氯化氢的物质的量为:1mol/L×0.05L=0.05mol,消耗镁、碳酸镁的物质的量都是:0.05mol÷2=0.025mol,加入镁的烧杯相对增重:0.025mol×24g/mol-0.025mol×2g/mol=0.55g,加入碳酸镁的烧杯相对增重:0.025mol×84g/mol-0.025mol×44g/mol=1g,因此天平不平衡;
B、当氧化钙、碳酸钙和盐酸恰好反应时,消耗的氯化氢的物质的量为:1mol/L×0.05L=0.05mol,消耗氧化钙、碳酸钙的物质的量都是:0.05mol÷2=0.025mol,加入氧化钙的烧杯相对增重:0.025mol×56g/mol=1.4g,加入碳酸钙的烧杯相对增重:0.025mol×100g/mol-0.025mol×44g/mol=1.4g,因此天平平衡;
C、当氧化钙、氢氧化钙和盐酸恰好反应时,消耗的氯化氢的物质的量为:1mol/L×0.05L=0.05mol,消耗氧化钙、氢氧化钙的物质的量都是:0.05mol÷2=0.025mol,加入氧化钙的烧杯相对增重:0.025mol×56g/mol=1.4g,加入氢氧化钙的烧杯相对增重:0.025mol×74g/mol=1.85g,因此天平不平衡;
D、当镁、氧化镁和盐酸恰好反应时,消耗的氯化氢的物质的量为:1mol/L×0.05L=0.05mol,消耗镁、氧化镁的物质的量都是:0.05mol÷2=0.025mol,加入镁的烧杯相对增重:0.025mol×24g/mol-0.025mol×2g/mol=0.55g,加入氧化镁的烧杯相对增重:0.025mol×40g/mol=1g,因此天平不平衡.
故选:B.
点评 当反应产生气体时,计算烧杯增重时,应该是加入的物质的质量减去生成气体的质量,如果不产生气体,烧杯增重即为加入物质的质量.

| A. | ②③④⑤ | B. | ①③⑤ | C. | ①③④⑤ | D. | ①②③⑤ |
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl=CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】(A)溶质可能是CaCl2与Ca(OH)2 (B)可能是CaCl2
(C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是排除了猜想(A),你认为排除猜想(A)的理由是酚酞溶液不变色,说明溶液不呈碱性,而猜想A的溶液呈碱性,所以可以排除.
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中, 逐滴加入碳酸钠溶液 | 生成白色沉淀 | 猜想(B)正确 |
| 先有气泡产生,后产生白色沉淀 | 猜想(C)正确 |
A.取反应后的溶液于试管中,滴加紫色石蕊试液变红色
B.取反应后的溶液于试管中,加入锌粉冒气泡
C.用洁净的玻璃棒蘸取反应后的溶液,涂抹在pH试纸上,测溶液的pH<7
D.取反应后的溶液于试管中,加入硝酸银溶液,生成白色沉淀.
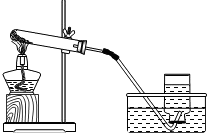 某同学在实验室用以下装置制备氧气并验证氧气的性质.
某同学在实验室用以下装置制备氧气并验证氧气的性质.