题目内容
14.在粗盐提纯的实验中,过滤后的食盐水仍含有CaCl2、Na2SO4等杂质,通过如下几个步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的BaC12溶液;③滴入稀盐酸至无气泡产生:④过滤(1)请填写出合理的操作顺序②①④③(填步骤序号)
(2)步骤①所发生反应的化学方程式CaCl2+Na2CO3=CaCO3↓+2NaCl、BaC12+Na2CO3=BaCO3↓+2NaCl.
分析 (1)根据硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子,进行分析解答.
(2)步骤①中,碳酸钠能与氯化钙、过量的氯化钡溶液反应,分别生成碳酸钙沉淀和氯化钠、碳酸钡沉淀和氯化钠,进行分析解答.
解答 解:(1)硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡;完全反应后,再进行过滤,最后再加入盐酸除去反应剩余的碳酸根离子,所以正确的顺序为:②①④③.
(2)步骤①中,碳酸钠能与氯化钙、过量的氯化钡溶液反应,分别生成碳酸钙沉淀和氯化钠、碳酸钡沉淀和氯化钠,所发生反应的化学方程式分别为CaCl2+Na2CO3=CaCO3↓+2NaCl、BaC12+Na2CO3=BaCO3↓+2NaCl.
故答案为:(1)②①④③;(2)CaCl2+Na2CO3=CaCO3↓+2NaCl、BaC12+Na2CO3=BaCO3↓+2NaCl.
点评 本题难度较大,考查了粗盐提纯中离子的除杂,除去多种杂质离子时,要考虑除杂的顺序、后面加入的试剂要能除去前面加入的过量的试剂.

练习册系列答案
相关题目
13.下列所示的四个图象,能正确反映对应变化关系的是( )
| A. |  电解水 | |
| B. |  向两份完全相同的稀盐酸中分别加入锌粉和铁粉 | |
| C. |  加热一定质量的高锰酸钾 | |
| D. |  向一定量的氢氧化钠溶液中加水稀释 |
14.下列图象不能正确反映对应变化关系的是( )
| A. | 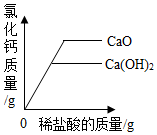 向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量 | |
| B. | 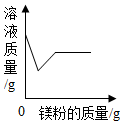 向一定质量氯化亚铁和氯化铝的混合溶液至加入镁粉至过量 | |
| C. |  向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量 | |
| D. |  向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量 |
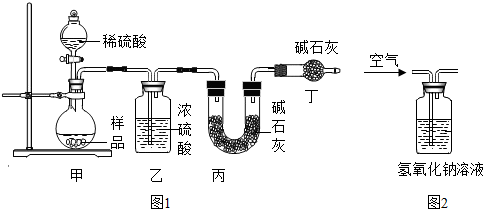

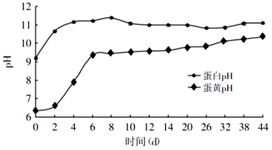 阅读下面科普短文(本文由网络文章改写).
阅读下面科普短文(本文由网络文章改写).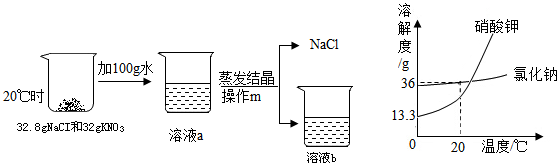
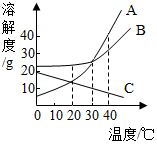 如图所示是A、B、C(均不含结晶水)三种物质的溶解度曲线,回答下列问题.
如图所示是A、B、C(均不含结晶水)三种物质的溶解度曲线,回答下列问题.