题目内容
石灰石是我省的主要矿产之一.学校研究性学小组为了测定当地矿山石灰石中碳酸钙的质量分数.取来了矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2 的质量/g | 1.76 | 3.52 | 4.4 | m |
(1)哪几次反应中矿石有剩余?
(2)试计算这种石灰石中碳酸钙的质量分数.
(3)上表中m值是 .
| 根据化学反应方程式的计算.. | |
| 专题: | 综合计算(图像型、表格型、情景型计算题). |
| 分析: | (1)观察并对比表格中的数据可知:第2次实验中加入的样品和生成二氧化碳的质量均为第一次实验的两倍,同时可以判断5g样品能够产生1.76g二氧化碳,而第3次加入样品比第2次加入的样品多5g,而生成的二氧化碳的质量只产生了4.4g﹣3.52g=0.88g,说明此时盐酸已完全反应,故3、4次实验中碳酸钙有剩余; (2)由(1)中的分析可以知道,实验1和实验2中样品中碳酸钙均完全反应,所以碳酸钙的质量分数可根据第1次或第2次实验中二氧化碳的质量求出.根据化学方程式得出各物质之间的质量比,列出比例式,即可求出参加反应的CaCO3的质量,然后再根据质量分数公式进行计算即可; (3)通过对表格中数据结合(1)的分析可以判定出m的值. |
| 解答: | 解:(1)观察并对比表格中的数据可知:第2次实验中加入的样品和生成二氧化碳的质量均为第一次实验的两倍,同时可以判断5g样品能够产生1.76g二氧化碳,而第3次加入样品比第2次加入的样品多5g,而生成的二氧化碳的质量只产生了4.4g﹣3.52g=0.88g,说明此时盐酸已完全反应,故3、4次实验中碳酸钙有剩余. (2)设第1次实验中样品中的碳酸钙的质量为x, CaCO3+2HCl═CaCl2+H2O+CO2↑ 100 44 x 1.76g
解之得:x=4g, 石灰石中碳酸钙的质量分数为: 答:石灰石中碳酸钙的质量分数为80%. (3)因为第3次反应已是完全反应,不再有气体产生,故第四次反应生成的气体质量的第三次的一样多,即m的值为4.4. 故答案为: (1)3、4两次; (2)80%; (3)4.4. |
| 点评: | 本题主要考查学生对完全反应的概念的认识,以及运用化学方程式和质量分数公式进行计算的能力. |

小亮同学学习化学后,对生活中的一些常识进行了总结,其中不合理的是( )
|
| A. | 吃松花皮蛋时,为了消除其中所含碱性物质的涩味,可加入少量食醋 |
|
| B. | 蜂窝煤比煤球燃烧更完全 |
|
| C. | 食用霉变的大米、花生等不会危害人体健康 |
|
| D. | 用燃烧的方法可以区别羊毛和涤纶 |
某温度下,将 3g A物质放入7g水中,得到 10g溶液,该溶液是( )
|
| A. | 饱和溶液 | B. | 不饱和溶液 | C. | 浓溶液 | D. | 无法确定 |
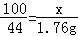
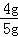 ×100%=80%.
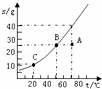
×100%=80%.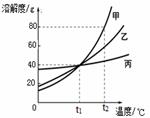 A.t1℃时,甲、乙、丙三者的溶解度相等
A.t1℃时,甲、乙、丙三者的溶解度相等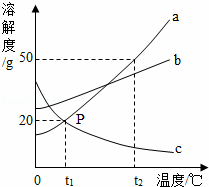
 处理才能排放到大气中
处理才能排放到大气中


 E
E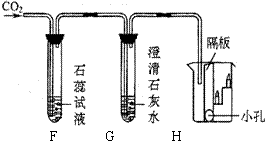 ⑶ 小彭同学设计了右图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,F中的现象是 ;
⑶ 小彭同学设计了右图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,F中的现象是 ; 二氧化碳具有的物理性质是 。
二氧化碳具有的物理性质是 。