题目内容
8.一包固体可能含有硫酸钠、氯化铜、碳酸钙和氯化钠中的一种或几种.根据以下实验得出的结论错误的是( )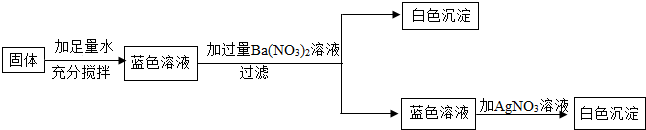
| A. | 一定有硫酸钠 | B. | 一定没有碳酸钙 | ||
| C. | 可能有氯化钠 | D. | 一定有氯化铜和氯化钠 |
分析 根据氯化铜在溶液中显蓝色,而碳酸钙难溶于水,碳酸根离子和硫酸根离子会与钡离子生成沉淀,且硫酸钡不会溶于硝酸,氯离子与银离子生成氯化银沉淀不溶于硝酸,进行分析.
解答 解:取该固体粉末少量,加足量水,搅拌,静置,得到蓝色溶液,说明存在氯化铜;因为碳酸钙难溶于水,故一定没有碳酸钙;溶液加入过量硝酸钡溶液生成白色沉淀,说明含有硫酸钠;而蓝色溶液中加入硝酸银溶液生成白色沉淀,则说明生成氯化银沉淀,故一定有氯化铜、硫酸钠,无法判定含有氯化钠;
故选:D.
点评 本题考查了常见物质的推断,解答本题的关键是要知道不溶于酸的白色沉淀有:硫酸钡和氯化银.

练习册系列答案
相关题目
19.下列实验操作正确的是( )
| A. | 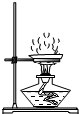 蒸发食盐水 | B. |  称量氢氧化钠 | C. |  稀释浓硫酸 | D. |  检验装置气密性 |
16.利用生物发光现象可检测“超微量钙”,此处“钙”是指( )
| A. | 分子 | B. | 原子 | C. | 元素 | D. | 单质 |
3.人类已能操纵原子制造分子,若用该方法制造葡萄糖(C6H12O6),不需要的原子是( )
| A. | 氮原子 | B. | 氧原子 | C. | 氢原子 | D. | 碳原子 |
20.下列有关认识错误的是( )
| A. | 常用于淡化海水的方法有蒸馏法、过滤法等 | |
| B. | 粗盐提纯为较纯净的食盐晶体的操作为:溶解、过滤、蒸发 | |
| C. | 通常在苦卤中加入熟石灰制取氢氧化镁 | |
| D. | 海水中的食盐用途广泛,例如侯德榜利用食盐为原料制得了纯碱 |
17.某久置的NaOH固体中水的质量分数为3.4%,Na2CO3质量分数为10.6%,其它均为NaOH.向20克的此样品中加入过量的稀盐酸,完全反应后再加入12克10%的NaOH溶液,恰好完全中和,则所得溶液中溶质质量为( )
| A. | 26.91 g | B. | 2.34g | C. | 29.25g | D. | 32.05g |
18.工业上冶炼金属锰的反应是3MnO2+4Al$\stackrel{高温}{→}$3Mn+2Al2O3,该反应中的还原剂是( )
| A. | MnO2 | B. | Al | C. | Mn | D. | Al2O3 |