题目内容
5.实验室常用如图甲装置制取气体,请你根据所学知识回答下列问题.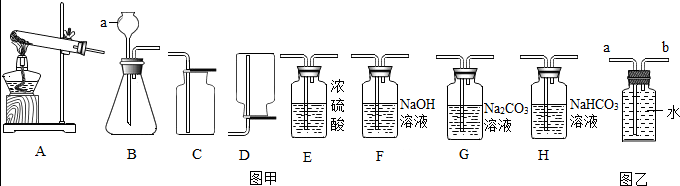
(1)装置D所采用的收集气体的方法是向下排空气法;
(2)实验室制取氧气时,选用上图中的收集装置是C(填字母序号).若改用图乙装置收集氧气,则气体应从b(填“a”或“b”) 进入.
(3)小明取一定浓度的盐酸与石灰石反应制取气体,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;将生成的气体通入澄清石灰水中,未见变浑浊,可能的原因是使用的盐酸浓度过大.
分析 (1)根据装置的特点来分析;
(2)根据氧气的性质来分析;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳.
解答 解:(1)装置D所采用的收集气体的方法是向下排空气法;故填:向下排空气法;
(2)氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,若改用图2装置收集氧气,则气体应从短管进入,因为氧气的密度比水小;故答案为:C;b;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,由于浓盐酸的挥发性,用盐酸和石灰石反应制取二氧化碳,挥发出的氯化氢气体,可能优先与石灰水中的氢氧化钙反应,如果将氢氧化钙耗尽,二氧化碳将不能使石灰水变浑浊;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;使用的盐酸浓度过大.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的除杂和干燥等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
16.下列有关金属材料说法错误的是( )
| A. | 黄铜的硬度比纯铜的硬度小 | |
| B. | 铝具有密度小和抗腐蚀性好的性能 | |
| C. | 铁制品与空气中的氧气、水蒸气接触容易生锈 | |
| D. | 金的化学性质很不活泼,在自然界中有单质的形式存在 |
20.向氧化铜和铁粉的混合物中,加入一定量的稀硫酸,反应停止后,过滤,除去不溶物.再向滤液中加一铁片,未看到铁片有任何变化.下列分析正确的是( )
| A. | 滤液中可能含有CuSO4和FeSO4 | B. | 滤液中一定不含有FeSO4和H2SO4 | ||
| C. | 滤出的不溶物中一定含有Cu | D. | 滤出的不溶物中一定含有Cu和Fe |
10.下列对宏观现象的微观解释错误的是( )
| A. | 氢氧化钠溶液和氢氧化钙溶液都能与二氧化碳反应,是因为它们溶液中的阴离子都是OH- | |
| B. | 温度计受热时水银柱上升,是因为汞原子受热时体积变大 | |
| C. | 20mL酒精和20mL水混合后体积小于40mL,是因为分子之间存在间隔 | |
| D. | 缉毒犬能根据气味发现毒品,是因为分子在不断地运动 |
15.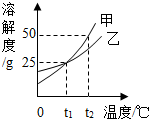 如图是甲、乙两种物质的溶解度曲线,下列说法中不正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列说法中不正确的是( )
 如图是甲、乙两种物质的溶解度曲线,下列说法中不正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列说法中不正确的是( )| A. | t2℃时,甲的溶解度为50g | |
| B. | t2℃时,75g甲的饱和溶液中加100g水得到20%的溶液 | |
| C. | t1℃时,甲、乙两种物质的饱和溶液中溶质质量分数相等 | |
| D. | t2℃时,各100g饱和溶液降温至t1℃,析出固体甲多于乙 |


